题目内容
2. 现欲用纯净的碳酸钙与稀盐酸反应制取二氧化碳气体,请回答:
现欲用纯净的碳酸钙与稀盐酸反应制取二氧化碳气体,请回答:(1)对于化学反应CaCO3+2HCl═CaCl2+CO2↑+H2O,在其他条件一定时,下列措施不能增大初始反应速率的是A(填序号,下同).
A.将盐酸的用量增加一倍
B.盐酸的浓度增加一倍,用量减半
C.适当加热
D.将块状碳酸钙换成粉末状固体
(2)为了降低上述化学反应的反应速率,欲向溶液中加入下列物质,你认为可行的是A.
A.蒸馏水
B.NaCl溶液
C.浓盐酸
(3)实验过程如图所示,分析EF段速率变化的原因该反应是放热反应,随着反应的进行,溶液温度升高、氢离子浓度降低,但温度对反应速率影响大于离子浓度降低.
分析 (1)增大反应物浓度、升高温度、增大反应物接触面积都加快反应速率;
(2)降低浓度、降低温度、减小反应物接触面积等都降低反应速率;
(3)反应物浓度越大反应速率越快,温度越高反应速率越快.
解答 解:(1)增大反应物浓度、升高温度、增大反应物接触面积都加快反应速率,
A.将盐酸的用量增加一倍,盐酸浓度不变,则反应速率不变,故选;
B.盐酸的浓度增加一倍,用量减半,反应物浓度增大,反应速率加快,故不选;
C.适当加热,增大活化分子百分数,反应速率加快,故不选;
D.将块状碳酸钙换成粉末状固体,增大反应物接触面积反应速率加快,故不选;
故选A;
(2)降低浓度、降低温度、减小反应物接触面积等都降低反应速率,
A.加入蒸馏水,氢离子浓度降低,反应速率减慢,故正确;
B.加入NaCl溶液,氢离子浓度降低,反应速率减慢,故正确;
C.加入浓盐酸,氢离子浓度增大,反应速率加快,故错误;
故选AB;
(3)反应物浓度越大反应速率越快,温度越高反应速率越快,开始时氢离子浓度大、溶液温度低,该反应是放热反应,随着反应的进行,溶液温度升高、氢离子浓度降低,但温度对反应速率影响大于离子浓度降低,所以反应速率增大,
故答案为:该反应是放热反应,随着反应的进行,溶液温度升高、氢离子浓度降低,但温度对反应速率影响大于离子浓度降低.
点评 本题考查化学反应速率影响因素,为高频考点,侧重考查学生知识运用及识图能力、分析判断能力,明确浓度、温度、反应物接触面积对反应速率影响原理是解本题关键,注意(3)题曲线变化原因,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.甲、乙、丙、丁四种易溶于水的物质分别由NH4+、Ba2+、Mg2+、H+、OH-、Cl-、HCO3-、SO42-中的不同阳离子和阴离子各一种组成.已知:
①向甲溶液中滴入AgNO3溶液有不溶于稀HNO3的白色沉淀生成;
②丙将溶液分别与其它三种物质的溶液混合,均有白色沉淀生成;
③1mol/L丁溶液中c(H+)=2mol/L.
下列结论不正确的是( )
①向甲溶液中滴入AgNO3溶液有不溶于稀HNO3的白色沉淀生成;
②丙将溶液分别与其它三种物质的溶液混合,均有白色沉淀生成;
③1mol/L丁溶液中c(H+)=2mol/L.
下列结论不正确的是( )
| A. | 甲溶液含有Cl- | B. | 乙溶液含有Mg2+ | C. | 丙溶液含有Ba2+ | D. | 丁溶液含有SO42- |
10.下列说法正确的是( )
| A. | 甲苯和液溴光照取代产物为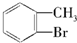 | |
| B. | 乙苯和氯气光照生成产物有11种 | |
| C. | 邻二甲苯和液溴在光照下取代产物可能为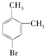 | |
| D. | 甲苯和氯气在光照条件下生成一氯代物有4种 |
7.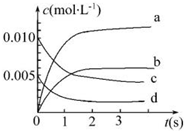 在2L密闭容器内,800℃时反应2NO(g)+O2(g)=2NO2(g)体系中,n(NO)随时间的变化如下表:
在2L密闭容器内,800℃时反应2NO(g)+O2(g)=2NO2(g)体系中,n(NO)随时间的变化如下表:
(1)上述反应在第5s时,NO的转化率为65%.
(2)如图中表示NO2变化曲线的是b.用O2表示0~2s内该反应的平均速率v=0.0015mol•L-1•S-1.
(3)能说明该反应已达到平衡状态的是bc.
a.v(NO2)=2v (O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变.
 在2L密闭容器内,800℃时反应2NO(g)+O2(g)=2NO2(g)体系中,n(NO)随时间的变化如下表:
在2L密闭容器内,800℃时反应2NO(g)+O2(g)=2NO2(g)体系中,n(NO)随时间的变化如下表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)如图中表示NO2变化曲线的是b.用O2表示0~2s内该反应的平均速率v=0.0015mol•L-1•S-1.
(3)能说明该反应已达到平衡状态的是bc.
a.v(NO2)=2v (O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变.
14.关于氨的下列叙述中,错误的是( )
| A. | 分别蘸有浓氨水和浓盐酸的两根玻璃棒靠近时有白烟生成 | |
| B. | 氨气极易溶解于水,因此可用来做喷泉实验 | |
| C. | 氯化铵受热分解有氨气生成,因此实验室可以用加热氯化铵的方法制备氨气 | |
| D. | 氨具有还原性,可以被氧化成NO |
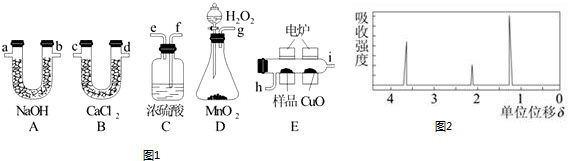
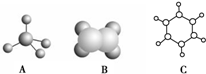 如图中A、B、C分别是三种有机物的结构模型:
如图中A、B、C分别是三种有机物的结构模型: