题目内容
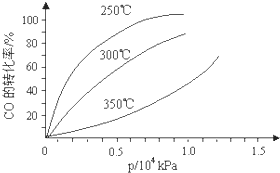 CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)?CH3OH(g).CO在不同温度下的平衡转化率与压强的关系如图所示.该反应△H
CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)?CH3OH(g).CO在不同温度下的平衡转化率与压强的关系如图所示.该反应△H考点:转化率随温度、压强的变化曲线
专题:化学平衡专题
分析:从横坐标上一点,画一条平行于纵坐标的虚线,看相同压强下不同温度时CO的平衡转化率,温度越低转化率越低,说明,升温时平衡向逆向移动.
解答:
解:从横坐标上一点0.5处,画一条平行于纵坐标的虚线,看相同压强下不同温度时CO的平衡转化率,温度越高转化率越低,说明,升温时平衡向逆向移动.
第二问:实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是工业生产要考虑速经济效益,要考虑速度和效率,压强越大需要的条件越高,花费越大.
故答案为:<;在1.3×104kPa下,CO的转化率已经很高,如果增加压强CO的转化率提高不大,而生产成本增加,经济效益低.
第二问:实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是工业生产要考虑速经济效益,要考虑速度和效率,压强越大需要的条件越高,花费越大.
故答案为:<;在1.3×104kPa下,CO的转化率已经很高,如果增加压强CO的转化率提高不大,而生产成本增加,经济效益低.
点评:本题考查了学生的识图能力,学会定一议二法分析图象得方法,这是学生必备的能力,题目难度中等.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案
相关题目
已知A、B、C、D、E分别为Ca(OH)2、Ca(HCO3)2、HCl、Ba(NO3)2、Na2CO3五种溶液中的一种.现将它们相互反应情况列表如下(表中“↓”表示生成沉淀;“↑”表示生成气体;“-”表示无现象)据此可判断C是( )
| A | B | C | D | E | |
| C | ↓ | ↓ | - | ↑ | - |
| B | ↓ | - | ↓ | - | - |
| A、HCl |
| B、Ca(HCO3)2 |
| C、Na2CO3 |
| D、Ba(NO3)2 |
已知下列热化学方程式,且b>a.Hg(l)+
O2(g)=HgO(s)△H=-a kJ?mol-1Zn(s)+
O2(g)=ZnO(s)△H=-b kJ?mol-1由此可知反应Zn(s)+HgO(s)=ZnO(s)+Hg(l)的焓变为( )
| 1 |
| 2 |
| 1 |
| 2 |
| A、-(b-a) kJ?mol-1 |
| B、+(b-a) kJ?mol-1 |
| C、(b-a) kJ?mol-1 |
| D、(b+a) kJ?mol-1 |
下面是4位同学对“化学与健康”这一话题发表的见解中,正确的是( )
| A、为了减肥,我每天只吃水果、蔬菜 |
| B、食用海产品可防治缺铁性贫血 |
| C、选择食物可调节人体细胞中的酸碱平衡 |
| D、我国应该禁止使用食物防腐剂 |
下列状态的物质,既能导电又属于电解质的是( )
| A、MgCl2晶体 |
| B、NaCl溶液 |
| C、液态酒精 |
| D、熔融的KOH |