题目内容
根据下列实验事实:①A+B2+═A2++B;②C+2H2O
C(OH)2+H2↑;③C2+的氧化性比A2+弱;④由B、D为电极组成的原电池,电极反应为:D2++2e-→D和B→B2++2e-.推断A、B、C、D的还原性由强到弱的顺序是( )
| ||
| A、C>A>B>D |
| B、C>D>A>B |
| C、A>C>B>D |
| D、C>B>A>D |
考点:氧化性、还原性强弱的比较
专题:
分析:根据同一化学反应中,还原剂的还原性大于还原产物的还原性分析解答.
解答:
解:①A+B2+=A2++B中,还原性A>B,
②C+2H2O=C(OH)2+H2↑中,C与冷水反应,则还原性:C>A,
③以B、D为电极与D的盐溶液组成原电池,电极反应为:D2++2e-→D和B→B2++2e-.还原性B>D,
所以这几种物质的还原性大小顺序为:C>A>B>D,
故选A.
②C+2H2O=C(OH)2+H2↑中,C与冷水反应,则还原性:C>A,
③以B、D为电极与D的盐溶液组成原电池,电极反应为:D2++2e-→D和B→B2++2e-.还原性B>D,
所以这几种物质的还原性大小顺序为:C>A>B>D,
故选A.
点评:本题以原电池原理为载体考查了氧化还原反应,根据同一化学反应中,还原剂的还原性大于还原产物的还原性分析解答即可,难度不大.

练习册系列答案
相关题目
向KBr和KI的混合溶液中通入足量的氯气后,溶液蒸干后并将剩余物灼烧,最后残余的物质是( )
| A、KCl |
| B、KCl和I2 |
| C、KCl和Br2 |
| D、KCl和KBr |
 以氨作为燃料的固体氧化物(含有O2-)燃料电池,具有固态结构、能量效率高的特点,另外氨气含氢量高,不含碳,易液化,方便运输和贮存,是很好的氢源载体.其工作原理如图所示,下列关于氨固体氧化物燃料电池的说法正确的是( )
以氨作为燃料的固体氧化物(含有O2-)燃料电池,具有固态结构、能量效率高的特点,另外氨气含氢量高,不含碳,易液化,方便运输和贮存,是很好的氢源载体.其工作原理如图所示,下列关于氨固体氧化物燃料电池的说法正确的是( )| A、电极a为电源的阴极 |
| B、固体氧化物作为电池工作的电解质,其作用是让电子在电池内移动 |
| C、电池工作时,在a电极接触面上发生的电极反应为2NH3+3O2--6e-=N2+3H2O |
| D、外电路的电流方向为从电极a流向电极b |
某种煤气的组成是:50%氢气、30%甲烷、10%一氧化碳、6%氮气和4%二氧化碳(均为体积分数).已知:
2H2(g)+O2(g)=2H2O (l)△H=-571.6kJ?mol-1
2CO(g)+O2(g)=2CO2(g)△H=-565.2kJ?mol-1
CH4(g)+2O2(g)=CO2(g)+H2O(l)△H=-890.3kJ?mol-1
则在标准状况下,224L该种煤气燃烧时放出的热量为( )
2H2(g)+O2(g)=2H2O (l)△H=-571.6kJ?mol-1
2CO(g)+O2(g)=2CO2(g)△H=-565.2kJ?mol-1
CH4(g)+2O2(g)=CO2(g)+H2O(l)△H=-890.3kJ?mol-1
则在标准状况下,224L该种煤气燃烧时放出的热量为( )
| A、2027.1kJ |
| B、4382.5 kJ |
| C、5094.1 kJ |
| D、5811.5 kJ |
下列有关化学用语正确的是( )
A、O原子的轨道表示式为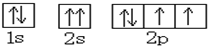 |
B、H2O的电子式为 |
| C、Ca原子的电子排布式为 1s22s22p63s23p63d2 |
D、K原子的原子结构示意图为 |
13 6 |
13 6 |
| A、该原子相对原子质量为12 |
| B、该原子原子核内中子数为13 |
| C、该原子中子数比质子数多7 |
| D、该原子核外电子数为6 |
X+的核外各层电子数分别为2、8,则X元素在周期表中的位置是( )
| A、第2周期第0族 |
| B、第3周期第ⅠA族 |
| C、第2周期第ⅠA族 |
| D、第2周期第ⅦA族 |
 将反应5IO3-+I-+6H+?3I2+3H2O设计成如图所示的原电池.开始时向甲烧杯中加入少量浓硫酸,电流计指针发生偏转,一段时间后,电流计指针回到零,再向甲烧杯中滴入几滴浓NaOH溶液,电流 计指针再次发生偏转.下列判断不正确的是( )
将反应5IO3-+I-+6H+?3I2+3H2O设计成如图所示的原电池.开始时向甲烧杯中加入少量浓硫酸,电流计指针发生偏转,一段时间后,电流计指针回到零,再向甲烧杯中滴入几滴浓NaOH溶液,电流 计指针再次发生偏转.下列判断不正确的是( )| A、开始加入少量浓硫酸时,乙中石墨电极上发生氧化反应 |
| B、开始加入少量浓硫酸时,同时在甲、乙烧杯中都加入淀粉溶液,只有乙烧杯中溶液变蓝 |
| C、电流计读数为零时,反应达到化学平衡状态 |
| D、两次电流计指针偏转方向相反 |