题目内容
反应物浓度均为0.10mol/L,下列各组反应中,反应速率最大的是( )
| A、0℃H2+F2═2HF |
| B、40℃H2+Cl2═2HCl |
| C、200℃H2+Br2(g)═2HBr |
| D、300℃H2+I2(g)═2HI |
考点:浓度、温度、催化剂对化学反应速率的影响
专题:
分析:根据反应物本身的性质分析,非金属性的强弱进行判断,元素的非金属性越强,对应的单质越活泼,与氢气反应越剧烈,化学反应速率最大.
解答:
解:反应物本身的性质分析是决定化学反应速率的主要原因;非金属性:F>Cl>Br>I,元素的非金属性越强,对应的单质越活泼,与氢气反应越剧烈,化学反应速率最大,则反应F2+H2=2HF的化学反应速率最大;
故选A.
故选A.
点评:本题考查反应速率的影响因素,难度不大,注意从非金属性的强弱的角度进行比较,答题时注意体会,该题很好的考查学生的分析能力和应用能力.

练习册系列答案
相关题目
下列存在顺反异构的是( )
| A、乙烯 | B、丙烯 |
| C、2-丁烯 | D、1-丁烯 |
下列物质属于非电解质的是( )
| A、C2H5OH |
| B、NaOH |
| C、NaCl |
| D、H2SO4 |
下列分子中的中心原子采取sp2杂化的是( )
①C6H6 ②C2H2 ③C2H4 ④C3H8 ⑤CO2 ⑥BeCl2⑦SO3 ⑧BF3.
①C6H6 ②C2H2 ③C2H4 ④C3H8 ⑤CO2 ⑥BeCl2⑦SO3 ⑧BF3.
| A、①②⑥⑦ | B、③⑤⑦⑧ |
| C、①③⑦⑧ | D、③⑤⑥⑦ |
化学工作者从有机反应:RH+C12(气)
RCl(液)+HCl(气)受到启发,提出的在农药和有机合成工业中可获得副产品盐酸的设想已成为现实.已知RCl难溶于水,产物HCl部分溶于RCl液体,指出从上述反应产物混合物中分离得到盐酸的最佳方法是( )
| 光 |
| A、蒸馏法 | B、水洗分液法 |
| C、过滤法 | D、有机溶剂萃取法 |
在同温同压下,10升N2和CO2的混合气体通过足量的Na2O2后,测得气体的体积是6升,原混合气中,CO2的体积分数是( )
| A、20% | B、40% |
| C、60% | D、80% |
已知同温度下,三种酸的电离平衡常数的大小关系为Ka(HX)>Ka(HY)>Ka(HZ),则物质的量浓度相同的三种盐NaX、NaY和NaZ溶液pH由大到小的顺序是( )
| A、NaX NaY NaZ |
| B、NaX NaZ NaY |
| C、NaY NaZ NaX |
| D、NaZ NaY NaX |
按如图所示装置,以石墨为电极电解氯化铜溶液,正确的是( )


| A、阴极为A |
| B、阳极电极反应式Cu2++2e-=Cu |
| C、在B极观察到有气泡,产生的气体能使湿润的淀粉-KI变蓝 |
| D、溶液中Cu2+移向B极 |
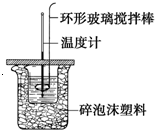 利用如图所示装置测定中和热的实验步骤如下:
利用如图所示装置测定中和热的实验步骤如下: