题目内容
芳香族含氧衍生物A经李比希法和质谱法分析得知其相对分子质量为136,其氧元素的质量分数为0.235.
(1)A的分子式是 .
(2)A如果能使溴的四氯化碳溶液褪色,请写出A的所有官能团的名称 .
(3)A如果属于酯类化合物,且苯环上只有一个取代基.则写出所有符合题意的结构简式 .
(4)A如果能与碳酸氢钠溶液反应放出气体.则写出有关反应方程式 .(任写1条即可)
(5)A如果既能发生银镜反应,又能与金属钠反应,但无酸性.请写出A的银镜反应方程式: .
(1)A的分子式是
(2)A如果能使溴的四氯化碳溶液褪色,请写出A的所有官能团的名称
(3)A如果属于酯类化合物,且苯环上只有一个取代基.则写出所有符合题意的结构简式
(4)A如果能与碳酸氢钠溶液反应放出气体.则写出有关反应方程式
(5)A如果既能发生银镜反应,又能与金属钠反应,但无酸性.请写出A的银镜反应方程式:
考点:有关有机物分子式确定的计算
专题:有机物分子组成通式的应用规律
分析:(1)芳香族含氧衍生物A的相对分子质量为136,其氧元素的质量分数为0.235,则分子中N(O)=
=2,分子中C、H原子总相对原子质量为136-32=104,分子中C原子最大数目=
=8…8,由于7个碳原子最多需要16个氢原子饱和,故A分子中含有8个C原子、8个H原子,则有机物A的分子式为C8H8O2;
(2)A如果能使溴的四氯化碳溶液褪色,则还含有碳碳双键,酚羟基;
(3)A如果属于酯类化合物,且苯环上只有一个取代基,则侧链为-CH2OOCH或-COOCH3、-OOCH2CH3;
(4)A如果能与碳酸氢钠溶液反应放出气体,则A含有-COOH,则A为苯乙酸或甲基苯甲酸(邻、间、对);
(5)A如果既能发生银镜反应,又能与金属钠反应,但无酸性,则A含有-CHO与醇羟基,A为 .
.
| 136×0.235 |
| 16 |
| 104 |
| 12 |
(2)A如果能使溴的四氯化碳溶液褪色,则还含有碳碳双键,酚羟基;
(3)A如果属于酯类化合物,且苯环上只有一个取代基,则侧链为-CH2OOCH或-COOCH3、-OOCH2CH3;
(4)A如果能与碳酸氢钠溶液反应放出气体,则A含有-COOH,则A为苯乙酸或甲基苯甲酸(邻、间、对);
(5)A如果既能发生银镜反应,又能与金属钠反应,但无酸性,则A含有-CHO与醇羟基,A为
 .
.解答:
解:(1)芳香族含氧衍生物A的相对分子质量为136,其氧元素的质量分数为0.235,则分子中N(O)=
=2,分子中C、H原子总相对原子质量为136-32=104,分子中C原子最大数目=
=8…8,由于7个碳原子最多需要16个氢原子饱和,故A分子中含有8个C原子、8个H原子,则有机物A的分子式为C8H8O2,
故答案为:C8H8O2;
(2)A的不饱和度为5,A如果能使溴的四氯化碳溶液褪色,则还含有碳碳双键,酚羟基,故答案为:碳碳双键、酚羟基;
(3)A如果属于酯类化合物,且苯环上只有一个取代基,则侧链为-CH2OOCH或-COOCH3、-OOCH2CH3,故A的结构简式为 、
、 、
、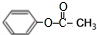 ,
,
故答案为: 、
、 、
、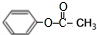 ;
;
(4)A如果能与碳酸氢钠溶液反应放出气体,则A含有-COOH,则A为苯乙酸或甲基苯甲酸(邻、间、对),苯乙酸与碳酸氢钠反应方程式为: +NaHCO3→
+NaHCO3→ +CO2↑+H2O,
+CO2↑+H2O,
故答案为: +NaHCO3→
+NaHCO3→ +CO2↑+H2O;
+CO2↑+H2O;
(5)A如果既能发生银镜反应,又能与金属钠反应,但无酸性,则A含有-CHO与醇羟基,A为 ,其银镜反应方程式为:
,其银镜反应方程式为: +2Ag(NH3)2OH
+2Ag(NH3)2OH
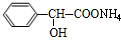 +2Ag↓+3NH3+H2O,
+2Ag↓+3NH3+H2O,
故答案为: +2Ag(NH3)2OH
+2Ag(NH3)2OH
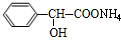 +2Ag↓+3NH3+H2O.
+2Ag↓+3NH3+H2O.
| 136×0.235 |
| 16 |
| 104 |
| 12 |
故答案为:C8H8O2;
(2)A的不饱和度为5,A如果能使溴的四氯化碳溶液褪色,则还含有碳碳双键,酚羟基,故答案为:碳碳双键、酚羟基;
(3)A如果属于酯类化合物,且苯环上只有一个取代基,则侧链为-CH2OOCH或-COOCH3、-OOCH2CH3,故A的结构简式为
 、
、 、
、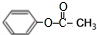 ,
,故答案为:
 、
、 、
、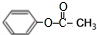 ;
;(4)A如果能与碳酸氢钠溶液反应放出气体,则A含有-COOH,则A为苯乙酸或甲基苯甲酸(邻、间、对),苯乙酸与碳酸氢钠反应方程式为:
 +NaHCO3→
+NaHCO3→ +CO2↑+H2O,
+CO2↑+H2O,故答案为:
 +NaHCO3→
+NaHCO3→ +CO2↑+H2O;
+CO2↑+H2O;(5)A如果既能发生银镜反应,又能与金属钠反应,但无酸性,则A含有-CHO与醇羟基,A为
 ,其银镜反应方程式为:
,其银镜反应方程式为: +2Ag(NH3)2OH
+2Ag(NH3)2OH| △ |
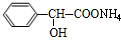 +2Ag↓+3NH3+H2O,
+2Ag↓+3NH3+H2O,故答案为:
 +2Ag(NH3)2OH
+2Ag(NH3)2OH| △ |
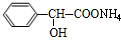 +2Ag↓+3NH3+H2O.
+2Ag↓+3NH3+H2O.
点评:本题考查有机物推断、限制条件同分异构体的书写等,计算确定A的分子式是关键,需要学生熟练掌握官能团的性质,侧重考查学生的计算能力、分析推理能力,难度中等.

练习册系列答案
相关题目
用46g乙醇(其中的氧用18),在浓硫酸存在条件下与足量的乙酸充分反应.下列有关叙述中不正确的是( )
| A、生成的水分子中含有18O |
| B、生成的乙酸乙酯中含有18O |
| C、可能生成88g乙酸乙酯 |
| D、不可能生成90g乙酸乙酯 |
固体粉末X中可能含有Fe、FeO、CuO、MnO2、KCl和K2CO3中的若干种.为确定该固体粉末的成分,某同学依次进行了以下实验:
①将X加入足量水中,得到不容物Y和溶液Z;
②取少量Y加入足量浓盐酸,加热,产生黄绿色气体,并有少量红色不容物;
③向Z溶液中滴加AgNO3溶液,生成白色沉淀;
④用玻璃棒蘸取Z于广范pH试纸上,试纸呈蓝色.
分析以上实验现象,下列结论正确的是( )
①将X加入足量水中,得到不容物Y和溶液Z;
②取少量Y加入足量浓盐酸,加热,产生黄绿色气体,并有少量红色不容物;
③向Z溶液中滴加AgNO3溶液,生成白色沉淀;
④用玻璃棒蘸取Z于广范pH试纸上,试纸呈蓝色.
分析以上实验现象,下列结论正确的是( )
| A、X中一定不存在FeO |
| B、不容物Y中一定含有FeO和CuO |
| C、Z溶液中一定存在K2CO3 |
| D、Y中一定存在MnO2 |
不外加任何试剂,鉴别下列5种物质的先后顺序是( )
①NaOH溶液 ②MgSO4溶液 ③BaCl2溶液 ④KNO3溶液 ⑤CuCl2溶液.
①NaOH溶液 ②MgSO4溶液 ③BaCl2溶液 ④KNO3溶液 ⑤CuCl2溶液.
| A、①②③④⑤ |
| B、②③⑤④① |
| C、⑤①②③④ |
| D、⑤③②①④ |
下列分离提纯物质的操作中,错误的是( )
| A、用过滤的方法除去食盐中的泥沙 |
| B、用分液的方法分离汽油和水 |
| C、用结晶的方法分离氯化钠和硝酸钾 |
| D、用加热的方法除去碳酸氢钠中混有的碘 |
不具备食品防腐作用的物质是( )
| A、醋 | B、糖 | C、食盐 | D、水 |
下列鉴别方法可行的是( )
| A、用银氨溶液鉴别HCOOCH3和CH3CHO |
| B、用溴水鉴别乙烯和乙炔 |
| C、用核磁共振氢谱鉴别1-溴丙烷和2-溴丙烷 |
| D、用KMnO4酸性溶液鉴别CH3CH=CHCH2OH和CH3CH2CH2CHO |
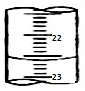 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下: