题目内容
某100mL硝酸和硫酸的混合液,其中硝酸的物质的量浓度为0.4mol/L,硫酸的物质的量浓度为0.1mol/L,向混合液中加入1.92g铜粉,微热,待充分反应后,试求产生气体的体积以及Cu2+的物质的量浓度.
考点:物质的量浓度的相关计算
专题:物质的量浓度和溶解度专题
分析:反应离子方程式为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,根据n=cV计算溶液中n(H+)、n(NO3-),根据n=
计算n(Cu),进行过量计算,根据不足量的物质计算n(NO)、n(Cu2+),进而计算NO的体积与Cu2+的物质的量浓度.
| m |
| M |
解答:
解:混合溶液中n(H+)=0.1L×0.4mol/L+0.1L×0.1mol/L×2=0.06mol,n(NO3-)=0.1L×0.4mol/L=0.04mol,n(Cu)=
=0.03mol,
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,
3 8 2
0.03mol 0.08mol 0.02mol
可知H+不足,完全反应,则生成n(NO)=
mol=0.015mol,V(NO)=0.015mol×22.4L/mol=0.336L,
n(Cu2+)=
=0.0225mol,则c(Cu2+)=
=0.225mol/L,
答:理论上生成的一氧化氮(标准状况下)的体积是0.672升,溶液中Cu2+物质的量浓度是0.225mol/L.
| 1.92g |
| 64g/mol |
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,
3 8 2
0.03mol 0.08mol 0.02mol
可知H+不足,完全反应,则生成n(NO)=
| 0.06mol×2 |
| 8 |
n(Cu2+)=
| 0.06mol×3 |
| 8 |
| 0.0225mol |
| 0.1L |
答:理论上生成的一氧化氮(标准状况下)的体积是0.672升,溶液中Cu2+物质的量浓度是0.225mol/L.
点评:本题考查化学方程式的计算,侧重于学生的分析能力和计算能力的考查,注意根据反应的离子方程式计算,明确物质的过量问题为解答该题的关键,难度不大.

练习册系列答案
相关题目
下列性质中,适用于分子晶体的是( )
| A、熔点1070℃,易溶于水,水溶液能导电 |
| B、能溶于CS2,熔点112.8℃,沸点444.6℃ |
| C、熔点97.81℃,质软,导电,密度0.97g/cm3 |
| D、熔点2200℃,不溶于水,熔融时不导电 |
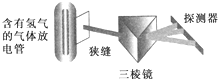 在实验室中用下列的装置可以得到氢原子光谱,实验证明该光谱为线状光谱,该光谱的发现在原子结构的认识过程中,有极为重要的意义,根据它产生了( )
在实验室中用下列的装置可以得到氢原子光谱,实验证明该光谱为线状光谱,该光谱的发现在原子结构的认识过程中,有极为重要的意义,根据它产生了( )| A、卢瑟福核式原子模型 |
| B、汤姆逊“葡萄干布丁”模型 |
| C、玻尔核外电子分层排布模型 |
| D、原子结构的量子力学模型 |