题目内容
11.1.0molPCl3和0.5molCl2充入体积不变的密闭容器中,一定条件下发生下述反应:PCl3(g)+Cl2(g)?PCl5(g);反应达到平衡时,PCl5为0.2mol;如果此时移走0.5molPCl3和0.25molCl2,在相同的温度下再达到平衡时,PCl5的物质的量( )| A. | 0.2mol | B. | 0.1mol | ||
| C. | 小于0.1mol | D. | 大于0.1mol,小于0.2mol |
分析 反应达到平衡时,PCl5为0.2mol,因体积、温度不变,移走反应物的物质的量为起始的一半,若平衡不移动,平衡时PCl5的物质的量为0.1mol,但由pV=nRT可知,n减小、压强减小,结合压强对平衡移动的影响来解答.
解答 解:移走反应物的物质的量为起始的一半,若平衡不移动,平衡时PCl5的物质的量为0.1mol,
但由pV=nRT可知,n减小、压强减小,
该反应为气体体积减小的反应,减小压强,平衡逆向移动,则达到新平衡时,PCl5的物质的量小于0.1mol,
故选C.
点评 本题考查化学平衡,为高频考点,把握压强与物质的量的关系、压强对平衡移动的影响为解答的关键,侧重分析与应用能力的考查,注意静态变化与动态变化的结合,题目难度不大.

练习册系列答案
相关题目
1.鉴别苯酚溶液、已烯和甲苯,可选用的最佳试剂( )
| A. | 溴水 | B. | FeCl3溶液 | C. | 新制Cu(OH)2悬浊液 | D. | 酸性KMnO4溶液 |
2.Fe(OH)3可用来制颜料、药物,作净水剂.现设计实验研究制备Fe(OH)3的方法.
资料:新制Fe(OH)3在溶液中存在两种电离:Fe3++3OH-?Fe(OH)3?H++FeO2-+H2O
(1)向3支盛有1mL 1.0mol•L-1 FeCl3溶液的试管中,分别加入3mL不同浓度的NaOH溶液,都产生红褐色沉淀.充分反应后,过滤,取滤液分成两等份,分别进行实验,实验记录如表:
①产生红褐色沉淀的离子方程式是Fe3++3OH-?Fe(OH)3↓.
②当c(NaOH)≥6.0 mol•L-1时,实验Ⅱ中溶液变红的原因是FeO2-+4H+?Fe3++2H2O、Fe3++3SCN-?Fe(SCN)3(用离子方程式表示).
(2)有同学提出可用某些盐与FeCl3反应制备Fe(OH)3.
①向1mL 1.0mol•L-1 FeCl3溶液中滴加1.0mol•L-1Na2CO3溶液,立即有大量气泡并有红褐色沉淀产生.有同学提出沉淀中可能含有碳酸盐.将沉淀过滤、洗涤后取样,加入少量稀盐酸,有无色气体产生,证明沉淀中含有碳酸盐.
②向1mL 1.0mol•L-1FeCl3溶液中滴加1.0mol•L-1Na2SO3溶液,溶液由黄色变为红色,无丁达尔效应,继续滴加Na2SO3溶液,最终得到红褐色沉淀.经检验沉淀中除Fe(OH)3外还含有FeSO3.产生FeSO3的原因是2Fe3++SO32-+H2O?2Fe2++SO42-+2H+、Fe2++SO32-?FeSO3↓.
(3)比较(1)和(2),制备Fe(OH)3的合理方法是1mL1.0mol•L-1FeCl3溶液与3mL浓度小于6.0mol•L-1的NaOH溶液(注明试剂和用量).
(4)FeSO4溶液仅与一种试剂反应也可制Fe(OH)3,该试剂的化学式是NaClO(写出一种即可).
资料:新制Fe(OH)3在溶液中存在两种电离:Fe3++3OH-?Fe(OH)3?H++FeO2-+H2O
(1)向3支盛有1mL 1.0mol•L-1 FeCl3溶液的试管中,分别加入3mL不同浓度的NaOH溶液,都产生红褐色沉淀.充分反应后,过滤,取滤液分成两等份,分别进行实验,实验记录如表:
 | 5.0 | 6.0 | 7.0 |
| 实验Ⅰ:滴入几滴KSCN溶液 | 不变红 | 不变红 | 不变红 |
| 实验Ⅱ:先加入过量稀硫酸,再滴入几滴KSCN溶液 | 不变红 | 变红 | 变红 |
②当c(NaOH)≥6.0 mol•L-1时,实验Ⅱ中溶液变红的原因是FeO2-+4H+?Fe3++2H2O、Fe3++3SCN-?Fe(SCN)3(用离子方程式表示).
(2)有同学提出可用某些盐与FeCl3反应制备Fe(OH)3.
①向1mL 1.0mol•L-1 FeCl3溶液中滴加1.0mol•L-1Na2CO3溶液,立即有大量气泡并有红褐色沉淀产生.有同学提出沉淀中可能含有碳酸盐.将沉淀过滤、洗涤后取样,加入少量稀盐酸,有无色气体产生,证明沉淀中含有碳酸盐.
②向1mL 1.0mol•L-1FeCl3溶液中滴加1.0mol•L-1Na2SO3溶液,溶液由黄色变为红色,无丁达尔效应,继续滴加Na2SO3溶液,最终得到红褐色沉淀.经检验沉淀中除Fe(OH)3外还含有FeSO3.产生FeSO3的原因是2Fe3++SO32-+H2O?2Fe2++SO42-+2H+、Fe2++SO32-?FeSO3↓.
(3)比较(1)和(2),制备Fe(OH)3的合理方法是1mL1.0mol•L-1FeCl3溶液与3mL浓度小于6.0mol•L-1的NaOH溶液(注明试剂和用量).
(4)FeSO4溶液仅与一种试剂反应也可制Fe(OH)3,该试剂的化学式是NaClO(写出一种即可).
19.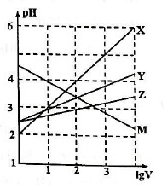 常温下取0.1mol•L-1的NaA和NaB两种盐溶液各1L,分别通入0.02mol CO2,发生如下反应:NaA+CO2+H2O?HA+NaHCO3、2NaB+CO2+H2O?2HB+Na2CO3.则HA和HB的1L溶液分别加水稀释至体积为VL时可能有如下的曲线,则下列说法正确的是( )
常温下取0.1mol•L-1的NaA和NaB两种盐溶液各1L,分别通入0.02mol CO2,发生如下反应:NaA+CO2+H2O?HA+NaHCO3、2NaB+CO2+H2O?2HB+Na2CO3.则HA和HB的1L溶液分别加水稀释至体积为VL时可能有如下的曲线,则下列说法正确的是( )
 常温下取0.1mol•L-1的NaA和NaB两种盐溶液各1L,分别通入0.02mol CO2,发生如下反应:NaA+CO2+H2O?HA+NaHCO3、2NaB+CO2+H2O?2HB+Na2CO3.则HA和HB的1L溶液分别加水稀释至体积为VL时可能有如下的曲线,则下列说法正确的是( )
常温下取0.1mol•L-1的NaA和NaB两种盐溶液各1L,分别通入0.02mol CO2,发生如下反应:NaA+CO2+H2O?HA+NaHCO3、2NaB+CO2+H2O?2HB+Na2CO3.则HA和HB的1L溶液分别加水稀释至体积为VL时可能有如下的曲线,则下列说法正确的是( )| A. | X是HA,M是HB | |
| B. | 常温下PH:NaA溶液>NaB溶液 | |
| C. | 对于$\frac{c({R}^{-})}{c(HR)c(O{H}^{-})}$的值(R代表A或B),一定存在HA>HB | |
| D. | 若常温下浓度均为0.1mol•L-1的NaA和HA的混合溶液的PH>7,则c(A-)>c(HA) |




 亚硝酸钠(NaNO,)被称为工业盐,在漂白、电镀等方面应用广泛.以木炭、浓硝酸、水和过氧化钠为原料制备亚硝酸钠的装置如图所示.
亚硝酸钠(NaNO,)被称为工业盐,在漂白、电镀等方面应用广泛.以木炭、浓硝酸、水和过氧化钠为原料制备亚硝酸钠的装置如图所示.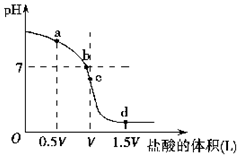 经测定某溶液中只含NH4+、Cl-、H+、OH-四种离子,已知这种溶液中含有一种或两种溶质.查资料表明等物质的量浓度的氨水和氯化铵溶液等体积混合后溶液显碱性,试完成下列各题.
经测定某溶液中只含NH4+、Cl-、H+、OH-四种离子,已知这种溶液中含有一种或两种溶质.查资料表明等物质的量浓度的氨水和氯化铵溶液等体积混合后溶液显碱性,试完成下列各题.