题目内容
3. 在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)?2NO2(g),随温度的升高,混合气体的颜色变深.
在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)?2NO2(g),随温度的升高,混合气体的颜色变深.回答下列问题:
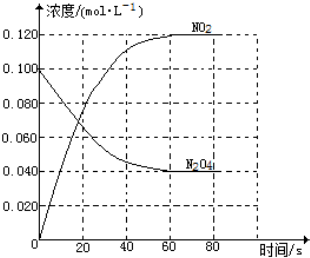
(1)反应的△H>0(填“>”或“<”);100℃时,体系中各物质浓度随时间变化如图所示.在0~60s时段,反应速率v(NO2)为0.002mol•L-1•s-1;达到平衡时N2O4的转化率为60%.
(2)100℃时达平衡后,改变反应温度为T,c(NO2)以0.0040mol•L-1•s-1的平均速率增加,经10s又达到平衡.
①T>100℃(填“>”或“<”),判断理由是c(NO2)增大平衡正向移动,正反应为吸热反应,故温度升高.
②计算温度T时反应的平衡常数K=1.28.
分析 (1)随温度的升高,混合气体的颜色变深,平衡向正反应方向移动,据此判断反应热;根据v=$\frac{△c}{△t}$计算在0~60s时段反应速率v(NO2);根据转化率=$\frac{反应消耗的浓度}{初始浓度}$×100%计算达到平衡时N2O4的转化率;
(2)①N2O4的浓度降低,平衡向正反应方向移动,由于正反应方向吸热,T>100℃;
②计算出T℃时N2O4、NO2的浓度,然后根据平衡常数的表达式计算出该温度下该反应的平衡常数.
解答 解:(1)随温度的升高,混合气体的颜色变深,化学平衡向正反应方向移动,即△H>0;
0~60s时段,NO2浓度变化为:0.12mol/L,v(NO2)=$\frac{0.12mol/L}{60s}$=0.002mol•L-1•s-1;
平衡时N2O4的浓度为0.040mol/L,则N2O4的转化率为:$\frac{0.10-0.04}{0.1}$×100%=60%,
故答案为:>;0.002;60%;
(2)①100℃时达平衡后,改变反应温度为T,c(NO2)以0.0040mol•L-1•s-1的平均速率增加,升高温度后平衡向正反应方向移动,由于正反应方向吸热,T>100℃,
故答案为:>;c(NO2)增大平衡正向移动,正反应为吸热反应,故温度升高;
②平衡时,c(NO2)=0.120mol•L-1+0.0040mol•L-1•s-1×10s=0.16mol•L-1,c(N2O4)=0.040mol•L-1-0.0040mol•L-1•s-1×$\frac{1}{2}$×10s=0.020mol•L-1,
则温度T时反应的平衡常数为:K=$\frac{(0.016)^{2}}{0.020}$=1.28,
故答案为:1.28.
点评 本题考查了化学平衡常数的计算,题目难度中等,明确图象曲线变化的含义为解答关键,注意掌握化学反应速率、化学平衡常数的概念及表达式,明确化学平衡及其影响为解答关键,试题培养了学生的分析能力及化学计算能力.

 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案| A. | NaCl溶液 | B. | NaOH溶液 | C. | NaHCO3溶液 | D. | NaHSO4溶液 |
| A. | 50mL 1mol•L-1 FeCl3溶液 | B. | 25mL 2mol•L-1 CaCl2溶液 | ||
| C. | 50mL 2mol•L-1 KCl溶液 |
| A. |  | B. |  | C. |  | D. |  |
| A. | 硫酸 | B. | 纯碱 | C. | 烧碱 | D. | 盐酸 |
| A. | 通入足量氨气:NH4+、SO42-、OH-、AlO2- | |
| B. | 加入足量Na2O2:Na+、Fe2+、SO42-、OH- | |
| C. | 加入过量稀硝酸:Al3+、Fe3+、H+、NO3-、SO42- | |
| D. | 加入过量漂白粉溶液:Ca2+、Fe2+、Cl-、ClO- |
| A. | K+、Na+、HSO3-、Cl- | B. | Na+、Ba2+、NO3-、Cl- | ||
| C. | K+、S2-、Cl-、CO32- | D. | K+、NH4+、Cl-、SO42- |
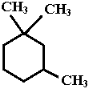 ,
,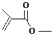 :
: .
.