题目内容
8. 铝热反应是铝的一个重要性质,该性质用途十分广泛,不仅被用于焊接钢轨,而且还常被用于冶炼高熔点的金属如钒、铬、锰等.
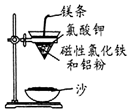
铝热反应是铝的一个重要性质,该性质用途十分广泛,不仅被用于焊接钢轨,而且还常被用于冶炼高熔点的金属如钒、铬、锰等.①某校化学兴趣小组同学,取磁性氧化铁按教材中的实验装置(如图)进行铝热反应,现象很壮观.取反应后的“铁块”溶于盐酸,向其中滴加KSCN溶液,发现溶液变血红色.出现这种现象的原因,除了可能混有没反应完的磁性氧化铁外,还有一个原因是
熔融的铁被空气中氧气氧化;
②若证明上述所得“铁块”中含有金属铝,可选择氢氧化钠溶液(填试剂名称),所发生反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑.
分析 ①滴加KSCN溶液,发现溶液变血红色,可知含铁离子,则可考虑生成的熔融的铁的还原性,可以被空气中的氧气氧化导致生成三价的铁;
②Al与NaOH溶液反应,而Fe不能.
解答 解:①铝热反应生成的熔融的铁具有很强的还原性,可以被空气中的氧气氧化导致生成三价的铁,
故答案为:熔融的铁被空气中氧气氧化;
②要证明“铁块”中含有金属铝,应利用铁和铝性质的差异性,即铁不能和碱反应,而铝可以,故应选择氢氧化钠溶液,与铝反应的离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案为:氢氧化钠溶液;2Al+2OH-+2H2O=2AlO2-+3H2↑.
点评 本题考查了铝热反应、性质实验方案的设计,题目难度中等,注意掌握铝热反应原理,明确性质实验方案设计与评价原则,侧重分析与实验能力的考查,题目难度中等.

练习册系列答案
相关题目
13.下列有关能量转化的说法正确的是( )
| A. | 动物体内的葡萄糖被氧化为CO2的过程是热能转化为化学能的过程 | |
| B. | 植物的光合作用是把太阳能转化为热能的过程 | |
| C. | 化石燃料和植物燃料燃烧时放出的能量均来源于太阳能 | |
| D. | 电解饱和食盐水是把化学能转化为电能 |
14.下列有关苯、乙酸、乙醇说法正确的是( )
| A. | 都易溶于水 | |
| B. | 苯易挥发不能用作溶剂 | |
| C. | 乙醇和乙酸反应的有机产物的同分异构体中属于酯类的有4种 | |
| D. | CH3CH2OH→CH3CHO发生了加成反应 |
16.自来水中因含有少量Cl-而不能用于溶液的配制,实验室为了除去自来水中的Cl-获得纯净水,可采用的方法是( )
| A. | 过滤法 | B. | 结晶法 | C. | 蒸馏法 | D. | 沉淀法 |
3.分类是科学研究的重要依据,下列物质分类不正确的是( )
| A. | 混合物:铝热剂、液氨、铝合金、酒精 | |
| B. | 化合物:干冰、冰水混合物、烧碱、小苏打 | |
| C. | 电解质:氯化钠、硫酸钡、氯化氢、水 | |
| D. | 同素异形体:活性炭、C60、石墨烯、金刚石 |
13. 莽草酸是一种合成治疗甲型H1N1流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中,下列关于这两种有机化合物的说法正确的是( )
莽草酸是一种合成治疗甲型H1N1流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中,下列关于这两种有机化合物的说法正确的是( )
 莽草酸是一种合成治疗甲型H1N1流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中,下列关于这两种有机化合物的说法正确的是( )
莽草酸是一种合成治疗甲型H1N1流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中,下列关于这两种有机化合物的说法正确的是( )| A. | 两种酸都能与溴水反应 | |
| B. | 两种酸遇三氯化铁溶液都显色 | |
| C. | 鞣酸分子与莽草酸分子相比多了两个碳碳双键 | |
| D. | 等物质的量的两种酸能消耗等量的NaOH |
20.下列电离方程式错误的是( )
| A. | NaHCO3=Na++H++CO32- | B. | NaHSO4=Na++H++SO42- | ||
| C. | H2SO4=2H++SO42- | D. | CH3COOH?CH3COO-+H+ |
17.同种元素的原子和离子,一定具有相同的( )
| A. | 质子数 | B. | 中子数 | C. | 电子数 | D. | 电子层数 |
18.298K时,向体积均为15.0mL、浓度均为1.00moL/L的氨水和NaHCO3溶液中分别滴加1.00mol/L的盐酸,溶液的pH与所加盐酸体积的关系如图所示.下列有关叙述正确的是( )

| A. | 两个滴定过程均可选择酚酞作指示剂 | |
| B. | 曲线a是NaHCO3溶液的滴定曲线 | |
| C. | 当V(盐酸)=4.00mol/L时,c(HCO3-)>c(NH4+)>c(CO32-) | |
| D. | 当V(盐酸)=15.00mol/L时,c(Na+)=c(NH4+) |