��Ŀ����
6�������������գ���1����NH3��N2H4�з��Ӹ�����Ϊ1��1 ʱ��ԭ������֮��Ϊ2��3������֮��Ϊ17��32��
��2������m gij���壬����˫ԭ�ӷ��ӹ��ɣ�����Ħ������ΪM g•mol-1����
�ٸ���������ʵ���Ϊ$\frac{m}{M}$mol��
�ڸ������ڱ�״���µ����Ϊ$\frac{22.4m}{M}$L��
�۸���������ˮ���γ�V L��Һ�������Ƿ�Ӧ��������Һ�����ʵ���Ũ��Ϊ$\frac{m}{MV}$mol•L-1��
��3����2mol/L��Mg��NO3��2��Һa mLϡ����b mL��ϡ�ͺ���Һ��NO3-�����ʵ���Ũ����$\frac{4a}{b}$mol•L-1��
��4���õ������0.2mol•L��1��BaCl2 ��Һ����ʹ��ͬ�����Na2SO4��KAl��SO4��2��Fe2��SO4��3������Һ�е�SO42����ȫ�����������������ε����ʵ���Ũ��֮��Ϊ6��3��2��
���� ��1����Ϸ���ʽ����ԭ����Ŀ֮�ȣ�������Ŀ��ȣ������ʵ�����ȣ�����m=nM��������֮�ȣ�
��2���ٸ���n=$\frac{m}{M}$�����������ʵ�����
�ڸ���V=nVm�������������
�۸���c=$\frac{n}{V}$������Һ���ʵ���Ũ�ȣ�
��3��2mol/L��Mg��NO3��2��Һ��NO3-�����ʵ���Ũ��Ϊ4mol/L������ϡ�Ͷ��ɼ���ϡ�ͺ�NO3-�����ʵ���Ũ�ȣ�
��4����������Ӧ��Ba2++SO42-=BaSO4���������Ȼ�����ȣ���SO42�������ʵ�����ȣ�
��� �⣺��1��NH3��N2H4�з��Ӹ�����Ϊ1��1 ʱ��ԭ������֮��Ϊ4��6=2��3���������ʵ�����ȣ�����֮��Ϊ17g/mol��32g/mol=17��32��
�ʴ�Ϊ��2��3��17��32��
��2�����������ʵ���Ϊ$\frac{mg}{Mg/mol}$=$\frac{m}{M}$mol���ʴ�Ϊ��$\frac{m}{M}$��
�ڱ���£����������Ϊ$\frac{m}{M}$mol��22.4L/mol=$\frac{22.4m}{M}$L���ʴ�Ϊ��$\frac{22.4m}{M}$��
�۸���������ˮ���γ�V L��Һ������Һ�����ʵ���Ũ��Ϊ$\frac{\frac{m}{M}mol}{VL}$=$\frac{m}{MV}$mol/L���ʴ�Ϊ��$\frac{m}{MV}$��
��3��2mol/L��Mg��NO3��2��Һ��NO3-�����ʵ���Ũ��Ϊ4mol/L������ϡ�Ͷ��ɣ�ϡ�ͺ�NO3-�����ʵ���Ũ��Ϊ$\frac{4mol/L��a��1{0}^{-3}L}{b��1{0}^{-3}L}$=$\frac{4a}{b}$mol/L���ʴ�Ϊ��$\frac{4a}{b}$��
��4����������Ӧ��Ba2++SO42-=BaSO4���������Ȼ�����ȣ���SO42�������ʵ�����ȣ���
V��c��Na2SO4��=2��V��c[KAl��SO4��2]=3��V��c[Fe2��SO4��3]
�ʣ�c��Na2SO4����c[KAl��SO4��2]��c[Fe2��SO4��3]=6��3��2��
�ʴ�Ϊ��6��3��2��
���� ���⿼�����ʵ����йؼ��㣬�������������ʵ���Ϊ���ĵļ��㹫ʽ��������ã���Ŀ�Ƚϻ�����

2Fe+3Br2�T2FeBr3��2FeBr3$\frac{\underline{\;\;��\;\;}}{\;}$2FeBr2+Br2����
���d��Һ�����100�桫120���D�У�������Сʱ��������Ӧ�������ܵ�һ�˳����л���ɫ��Ƭ״�廯����80g��
��ش�
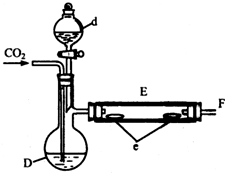
��1������d�����Ʒ�Һ©����
��2�������CO2���������E�з�������Ӧ���京��������ΪFe3O4�������ò����к��˸�����û�ѧ�������飮���з�����������B��
A��ȡ�����������Թ��м���ϡ���ᣬ�ټ���KSCN��Һ
B��ȡ����������Ӳ�ʴ��Թ��У�ͨ���������ž���������ȣ���CuSO4�������ɵ�ˮ����
C���ô����������������ܷ�����
D��ȡ�����������Թ��м�������ˮ�����˿��Ƿ��к�ɫ������
��3��Ϊ��ֹ��Ⱦ������ʵ��ʱӦ��F������ʢ��NaOH��Һ��β������װ�ã���Ӧ�Ļ�ѧ����ʽ��2NaOH+Br2=NaBr+NaBrO+H2O��
��4��ȡ��Ʒ10g���Ƴ�250mL��Һ��ȡ��25.00mL������KMnO4��Һ�ζ���Һ�е�Fe2+����ȥ0.03000mol/L����KMnO4��Һ25.00mL�����Ʒ�Ĵ���Ϊ81%��
��5�����ó�ȥ���ʺ��FeBr2������֤Cl2��Fe3+��Br2��������ǿ����������Ƶ�ʵ�������Ԥ�Ƶ�ʵ�������ʵ����ۣ�������ǿ������д�����б��ո��ڣ�
| ʵ����� | ʵ������ | ������ǿ�� |
| ��ȡһ����FeBr2����ˮ�������������Σ���ˮ����ͨ������������������KSCN��Һ | ��Һ��Ѫ��ɫ | ��Cl2��Fe3+ Br2��Fe3+ |
| ��ȡ����FeBr2����ˮ�����������ˮ����ͨ���������������������Ȼ�̼���� | �����Ȼ�̼����غ�ɫ | Cl2��Br2 |
| A�� | HCl | B�� | NaCl | C�� | H2 | D�� | CO2 |
| A�� | �������� | B�� | ���������� | C�� | �������� | D�� | ������ʽ�� |
| A�� | Cu2+ | B�� | Fe2+ | C�� | Cl2 | D�� | Cl- |
 ʵ�����Ʊ�����������Ҫ�������£�
ʵ�����Ʊ�����������Ҫ�������£�