题目内容
11.将Al和Na的单质同时加入到一定量的水中,充分反应后,发现既无沉淀生成又无固体残留物存在,请用两个化学反应方程式表示其变化:(1)2Na+2H2O=2NaOH+H2↑,(2)2Al+2NaOH+2H2O=2NaAlO2+3H2↑.分析 Al和Na的单质同时加入到一定量的水中,钠先与水反应生成氢氧化钠和氢气,氢氧化钠溶液再与铝反应生成偏铝酸钠和氢气,据此解答.
解答 解:Al和Na的单质同时加入到一定量的水中,钠先与水反应生成氢氧化钠和氢气,化学方程式:2Na+2H2O=2NaOH+H2↑,氢氧化钠溶液再与铝反应生成偏铝酸钠和氢气,化学方程式:2Al+2NaOH+2H2O=2NaAlO2+3 H2↑.
故答案为:2Na+2H2O=2NaOH+H2↑;2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
点评 本题考查了元素化合物知识,熟悉钠及氢氧化钠、铝的性质是解题关键,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
6.欲除去铁粉中少量的铝粉,可选用的试剂是( )
| A. | 水 | B. | 氢氧化钠溶液 | C. | 稀硫酸 | D. | 稀硝酸 |
16.下列各组单质中,前者在一定的条件下能将后者从其化合物中置换出来的是( )
①Al、Fe ②Cl2、S ③Mg、C ④H2、Cu ⑤Cl2、H2.
①Al、Fe ②Cl2、S ③Mg、C ④H2、Cu ⑤Cl2、H2.
| A. | 只有①③ | B. | 只有②④ | C. | 只有①②③④ | D. | ①②③④⑤ |
3.下列说法正确的是( )
| A. | 用广泛pH试纸测得氯水的pH=5.2 | |
| B. | 若H2O2分解产生1molO2,理论上转移的电子数约为4×6.02×1023 | |
| C. | 在氧化还原反应中,还原剂得到电子总数等于氧化剂失去电子的总数 | |
| D. | Mg在CO2中燃烧生成MgO和C.在该反应条件下,Mg的还原性强于C的 |
20.中药狼把草的成分之一M具有消炎杀菌作用,M的结构如图所示:下列叙述正确的( )
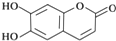

| A. | M的分子式是C9H6O4 | |
| B. | 1molM最多能与2molBr2发生反应 | |
| C. | M与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H4O5Na4 | |
| D. | 1molM与足量NaHCO3反应能生成2molCO2 |

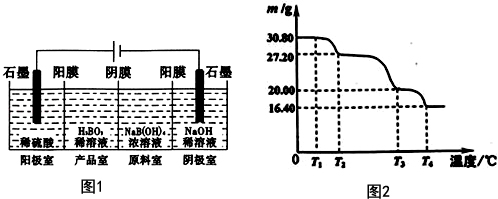 硼酸(H3BO3)与铝酸(H3AlO3)结构相似,可写成B(OH)3.
硼酸(H3BO3)与铝酸(H3AlO3)结构相似,可写成B(OH)3.