题目内容
4.已知可逆反应CO+H2O(g)?CO2+H2,依题意回答下列问题:(1)830K时,若起始时:c(CO)=2mol/L,c(H2O)=3mol/L,平衡时CO的转化率为60%,水蒸气的体积分数为30%;K值为1.
(2)830K时,若只将起始时,c(H2O)改为6mol/L,则CO的转化率为75%.
(3)若830K时,起始浓度c(CO)=a mol/L,c(H2O)=b mol/L,H2的平衡浓度c(H2)=c mol/L
①a、b、c之间的关系式是ab=c(a+b).
②当a=b时,a与c的关系式为a=2c.
分析 (1)830K时,若起始时:c(CO)=2mol/L,c(H2O)=3mol/L,平衡时CO的转化率为60%,即转化的CO为2mol/L×60%=1.2mol/L,则
CO+H2O(g)?CO2+H2
开始 2 3 0 0
转化 1.2 1.2 1.2 1.2
平衡 0.8 1.8 1.2 1.2
K为生成物浓度幂之积与反应物浓度幂之积的比;
(2)温度不变,K不变,若只将起始时,c(H2O)改为6mol/L,则
CO+H2O(g)?CO2+H2
开始 2 6 0 0
转化 x x x x
平衡 2-x 6-x x x
K=$\frac{x×x}{(2-x)(6-x)}$,
(3)若830K时,起始浓度c(CO)=a mol/L,c(H2O)=b mol/L,H2的平衡浓度c(H2)=c mol/L
CO+H2O(g)?CO2+H2
开始 a b 0 0
转化 c c c c
平衡 a-c b-c c c
a=b时,$\frac{c×c}{(a-c)×(a-c)}$=K,以此来解答.
解答 解:(1)830K时,若起始时:c(CO)=2mol/L,c(H2O)=3mol/L,平衡时CO的转化率为60%,即转化的CO为2mol/L×60%=1.2mol/L,则
CO+H2O(g)?CO2+H2
开始 2 3 0 0
转化 1.2 1.2 1.2 1.2
平衡 0.8 1.8 1.2 1.2
K=$\frac{1.2×1.2}{0.8×1.8}$=1,水蒸气的体积分数为$\frac{1.8}{0.8+1.8+1.2+1.2}$×100%=30%,
故答案为:30%;1;
(2)温度不变,K不变,若只将起始时,c(H2O)改为6mol/L,则
CO+H2O(g)?CO2+H2
开始 2 6 0 0
转化 x x x x
平衡 2-x 6-x x x
K=$\frac{x×x}{(2-x)(6-x)}$=1,解得x=1.5,
则CO的转化率为$\frac{1.5mol}{2mol}$×100%=75%,
故答案为:75%;
(3)若830K时,起始浓度c(CO)=a mol/L,c(H2O)=b mol/L,H2的平衡浓度c(H2)=c mol/L
CO+H2O(g)?CO2+H2
开始 a b 0 0
转化 c c c c
平衡 a-c b-c c c
①由K可知,$\frac{c×c}{(a-c)×(b-c)}$=1,则a、b、c之间的关系式是ab=c(a+b),故答案为:ab=c(a+b);
②当a=b时,a与c的关系式为a=b时,$\frac{c×c}{(a-c)×(a-c)}$=K=1,则a与c的关系式为a=2c,故答案为:a=2c.
点评 本题考查化学平衡的计算,为高频考点,把握平衡三段法、转化率及K的计算为解答的关键,侧重分析与计算能力的考查,注意(3)为解答的难点,题目难度不大.


(1)B装置的作用是检验产物中是否有水生成.
(2)实验中,观察到C中无明显现象,D中有白色沉淀生成,可确定产物中一定有SO2气体产生,写出D中发生反应的离子方程式SO2+H2O2+Ba2+=BaSO4↓+2H+.若去掉C,能否得出同样结论否(填“是”或“否”),原因是若有SO3也有白色沉淀生成.
(3)A中固体完全分解后变为红棕色粉末,某同学设计实验验证固体残留物仅为Fe2O3,而不含FeO,请帮他完成表中内容.(试剂,仪器和用品自选)
| 实验步骤 | 预期现象 | 结论 |
| 取少量A中残留物于试管中,加入适量稀硫酸,充分振荡使其完全溶解;将溶液分成两份,分别滴加高锰酸钾溶液、KSCN溶液 | 若高锰酸钾溶液不褪色,加入KSCN溶液后变红 | 固体残留物仅为Fe2O3 |
(5)结合上述实验现象,完成硫酸亚铁铵在500℃时隔绝空气加热完全分解的化学方程式2(NH4)2Fe(SO4)2═Fe2O3+2 NH3↑+N2↑+4SO2↑+5H2O.

已知:①Cu2O+2H+=Cu+Cu2++H2O
②几种氢氧化物开始沉淀和完全沉淀的pH如表:
| 氢氧化物 | Al(OH)3 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 |
| 开始沉淀的pH | 4.0 | 5.8 | 1.1 | 5.4 |
| 完全沉淀的pH | 5.2 | 8.8 | 3.2 | 6.7 |
(1)固体A 主要由两种物质组成,其化学式为SiO2、Cu.
(2)酸浸、过滤后,滤液中铁元素的存在形式为Fe2+(填离子符号),生成该离子的离子方程式为2Fe3++Cu=2Fe2++Cu2+.
(3)沉淀B的化学式为Fe(OH)3,氧化过程中发生反应的离子方程式为2Fe2++ClO-+2CO32-+3H2O=Fe(OH)3↓+Cl-+2CO2↑.
(4)加NaOH调节溶液pH的范围是5.2≤pH<5.4,工业上对沉淀B、沉淀C的利用应采取的处理方法是加热分解得到相应的氧化物,用于冶炼铁和铝.
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的化学平衡常数表达式为K=$\frac{c(CO)c({H}_{2}O)}{c(C{O}_{2})c({H}_{2})}$;
(2)反应是吸热反应.能判断该反应是否达到化学平衡状态的依据是bc.
a.容器中压强不变
b.混合气体中c(CO)不变
c.v正(H2)=v逆(H2O)
d.c(CO2)=c(CO)
(3)某温度下,平衡浓度符合下式:c(CO2)c(CH2)=c(CO)c(H2O),试判断此时的温度为830℃

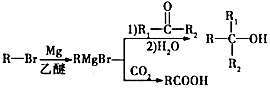
 ,其反应类型为取代反应.
,其反应类型为取代反应. .
. (写结构简式).
(写结构简式).
 .
. .
.