题目内容
E和M均为生活中常见的金属元素.现有如下反应关系:
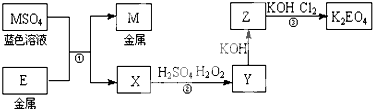
(1)反应①的反应类型是 (填序号).
a.氧化还原反应 b.复分解反应 c.置换反应
(2)Y溶液可使KSCN溶液显红色.向X的溶液中加入NaOH溶液,会出现的现象是: .
(3)K2EO4为高效绿色净水剂,可通过反应③制得,反应③的化学方程式是 .
(4)用K2EO4和Zn作原料的电池是一种新型可充电电池,该电池长时间保持稳定的放电电压.其总反应可写成:3Zn+2K2EO4+8H2O
3Zn(OH)2+2E(OH)3+4KOH,则放电时正极的电极反应式为: .放电时消耗32.5g Zn时转移 mol电子.

(1)反应①的反应类型是
a.氧化还原反应 b.复分解反应 c.置换反应
(2)Y溶液可使KSCN溶液显红色.向X的溶液中加入NaOH溶液,会出现的现象是:
(3)K2EO4为高效绿色净水剂,可通过反应③制得,反应③的化学方程式是
(4)用K2EO4和Zn作原料的电池是一种新型可充电电池,该电池长时间保持稳定的放电电压.其总反应可写成:3Zn+2K2EO4+8H2O
| 放电 |
| 充电 |
考点:无机物的推断
专题:推断题
分析:E利M均为生活中常见的金属元素,MSO4为蓝色溶液,铜盐为蓝色溶液,所以M为Cu,E和硫酸铜发生置换反应生成铜和硫酸盐X,X和稀硫酸、双氧水发生反应生成Y,E能被双氧水氧化,说明E为变价金属,E为生活中常见金属,则E为Fe,X是FeSO4,硫酸亚铁被双氧水氧化生成Fe2(SO4)3,所以Y是Fe2(SO4)3,硫酸铁和氢氧化钾反应生成Fe(OH)3和硫酸钾,Z能被氯气氧化,则Z是Fe(OH)3,结合物质的性质分析解答.
解答:
解:E利M均为生活中常见的金属元素,MSO4为蓝色溶液,铜盐为蓝色溶液,所以M为Cu,E和硫酸铜发生置换反应生成铜,和硫酸盐X,X和稀硫酸、双氧水发生反应生成Y,E能被双氧水氧化,说明E为变价金属,E为生活中常见金属,则E为Fe,X是FeSO4,硫酸亚铁被双氧水氧化生成Fe2(SO4)3,所以Y是Fe2(SO4)3,硫酸铁和氢氧化钾反应生成Fe(OH)3和硫酸钾,Z能被氯气氧化,则Z是Fe(OH)3,
(1)反应①是一种单质和一种化合物反应生成另外的单质和化合物,属于置换反应,故答案为:c;
(2)Y的溶液可使KSCN溶液显红色,说明Y中含有铁离子,X中含有亚铁离子,向X的溶液中加入NaOH溶液,生成白色沉淀并迅速变成灰绿色,最后变为红褐色,故答案为:生成白色沉淀并迅速变成灰绿色,最后变为红褐色;
(3)K2FeO4为高效绿色净水剂,可通过反应③制得,氢氧化铁和氢氧化钾和氯气反应生成高铁酸钾和氯化钾,反应方程式为:2Fe(OH)3+10KOH+3Cl2=2K2FeO4+8H2O+6KCl,故答案为:2Fe(OH)3+10KOH+3Cl2=2K2FeO4+8H2O+6KCl;
(4)根据电池的总反应可知,高铁电池放电时必定是锌在负极失去电子,电极反应式为Zn-2e-+2OH-=Zn(OH)2,高铁酸钾在正极得到电子,电极反应式为FeO42-+4H2O+3e-=Fe(OH)3+5OH-,根据电极反应式Zn-2e-+2OH-=Zn(OH)2,每消耗1molZn,转移2mol电子,放电时消耗32.5gZn,即Zn的物质的量=
=0.5mol,可知转移电子数为1mol,故答案为:FeO42-+4H2O+3e-=Fe(OH)3+5OH;1.
(1)反应①是一种单质和一种化合物反应生成另外的单质和化合物,属于置换反应,故答案为:c;
(2)Y的溶液可使KSCN溶液显红色,说明Y中含有铁离子,X中含有亚铁离子,向X的溶液中加入NaOH溶液,生成白色沉淀并迅速变成灰绿色,最后变为红褐色,故答案为:生成白色沉淀并迅速变成灰绿色,最后变为红褐色;
(3)K2FeO4为高效绿色净水剂,可通过反应③制得,氢氧化铁和氢氧化钾和氯气反应生成高铁酸钾和氯化钾,反应方程式为:2Fe(OH)3+10KOH+3Cl2=2K2FeO4+8H2O+6KCl,故答案为:2Fe(OH)3+10KOH+3Cl2=2K2FeO4+8H2O+6KCl;
(4)根据电池的总反应可知,高铁电池放电时必定是锌在负极失去电子,电极反应式为Zn-2e-+2OH-=Zn(OH)2,高铁酸钾在正极得到电子,电极反应式为FeO42-+4H2O+3e-=Fe(OH)3+5OH-,根据电极反应式Zn-2e-+2OH-=Zn(OH)2,每消耗1molZn,转移2mol电子,放电时消耗32.5gZn,即Zn的物质的量=
| 32.5g |
| 65g/mol |
点评:本题铁及其化合物为载体考查了无机物的推断,以MSO4的颜色为突破口采用正向推导的方法进行推断,结合物质的性质分析解答,难度中等.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
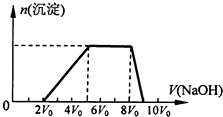 某混合溶液中可能含有的离子如表所示:
某混合溶液中可能含有的离子如表所示:
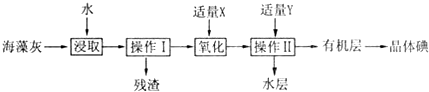

 (1)药品分为处方药和非处方药.处方药是指必须在医生监控或指导下使用的药物,用符号
(1)药品分为处方药和非处方药.处方药是指必须在医生监控或指导下使用的药物,用符号