题目内容
常温时,下列溶液的pH等于8或大于8的是( )
| A、0.1 mol?L-1的NaOH溶液滴定稀盐酸,用酚酞做指示剂滴定到终点 |
| B、pH=6的醋酸用水稀释100倍 |
| C、pH=10的氢氧化钠溶液稀释1000倍 |
| D、0.1 mol?L-1的硫酸100 mL跟0.2 mol?L-1 NaOH溶液100 mL完全反应 |
考点:pH的简单计算
专题:电离平衡与溶液的pH专题
分析:A.酚酞的变色范围pH为8~10;
B.酸稀释只能无限接近中性,但一定为酸性,酸稀释10n倍,若为强酸pH值变化n个单位,若为弱酸变化小于n个单位;
C.碱稀释只能无限接近中性,但一定为碱性,碱稀释10n倍,若为强碱pH值变化n个单位,若为弱碱变化小于n个单位;
D.先根据酸、碱反应计算剩余物质的酸碱性,再根据溶液中氢离子浓度计算溶液的pH值.
B.酸稀释只能无限接近中性,但一定为酸性,酸稀释10n倍,若为强酸pH值变化n个单位,若为弱酸变化小于n个单位;
C.碱稀释只能无限接近中性,但一定为碱性,碱稀释10n倍,若为强碱pH值变化n个单位,若为弱碱变化小于n个单位;
D.先根据酸、碱反应计算剩余物质的酸碱性,再根据溶液中氢离子浓度计算溶液的pH值.
解答:
解:A.酚酞的变色范围PH为8~10,所以0.1mol?L-1的NaOH溶液滴定稀盐酸,用酚酞做指示剂滴定到终点时,溶液的pH值等于8或大于8,故A正确;
B.pH=6的醋酸用水稀释100倍时,接近中性,溶液的PH值<7,故B错误;
C.pH=10的氢氧化钠溶液稀释1000倍时,溶液的pH值略大于7,接近于7,故C错误;
D.设0.1mol?L-1的硫酸100mL需要0.2mol?L-1NaOH溶液x.
硫酸和氢氧化钠的反应方程式为:
2NaOH+H2SO4=Na2SO4+2H2O
2mol 1mol
0.2x 0.01mol
x=0.1L=100mL,所以恰好中和,PH=7,故D错误;
故选A.
B.pH=6的醋酸用水稀释100倍时,接近中性,溶液的PH值<7,故B错误;
C.pH=10的氢氧化钠溶液稀释1000倍时,溶液的pH值略大于7,接近于7,故C错误;
D.设0.1mol?L-1的硫酸100mL需要0.2mol?L-1NaOH溶液x.
硫酸和氢氧化钠的反应方程式为:
2NaOH+H2SO4=Na2SO4+2H2O
2mol 1mol
0.2x 0.01mol
x=0.1L=100mL,所以恰好中和,PH=7,故D错误;
故选A.
点评:本题考查了pH的简单计算,题目难度中等,注意酸、碱溶液无限稀释时,溶液的pH值只能无限接近于7,但酸不能变为碱,碱不能变为酸.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列有关SO2说法中不正确的是( )
| A、被酸雨污染的农田及湖泊可洒石灰石粉末,减轻其危害 |
| B、在BaCl2溶液中通入SO2气体,溶液仍澄清,滴入3%过氧化氢溶液有白色沉淀 |
| C、二氧化硫具有强还原性,故不能用浓硫酸干燥 |
| D、二氧化硫能漂白某些物质,加热后可恢复原色 |
下列各组离子一定能在指定环境中大量共存的是( )
| A、含有大量SO42-的溶液:K+、Cu2+、Cl-、NO3- |
| B、在pH=1的溶液中:NO3-、SO42-、Na+、NH4 |
| C、在由水电离出的c(H+)=1×10-12mol/L的溶液中:Fe3+、ClO-、Na+、SO42- |
| D、滴加石蕊试液显红色的溶液:K+、Al3+、NO3-、CH3COO- |
与键线式为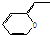 的物质互为同分异构体的是( )
的物质互为同分异构体的是( )
 的物质互为同分异构体的是( )
的物质互为同分异构体的是( )A、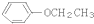 |
B、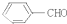 |
C、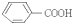 |
D、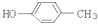 |
与Mg相比,Al( )
| A、金属性更大 |
| B、更难与碱反应 |
| C、半径更大 |
| D、更难与酸反应 |
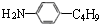 可能有4种异构体,它们是:
可能有4种异构体,它们是: