题目内容
4.用NA表示阿伏加德罗常数的值,下列判断正确的是( )| A. | 44gN2O含有的氮原子数目为NA | |
| B. | 常温常压下,22.4 L N2含有的分子数目为NA | |
| C. | 1 mol Mg变为Mg2+时失去的电子数目为2NA | |
| D. | lmol•L-1K2CO3,溶液中含有的钾离子数目为NA |
分析 A.根据n=$\frac{m}{M}$计算出44gN2O的物质的量,1molN2O中含有2mol氮原子;
B.常温常压下,不能使用标准状况下的气体摩尔体积计算;
C.镁为2价金属,1mol镁完全反应失去2mol电子;
D.缺少溶液体积,无法计算溶液中含有钾离子的数目.
解答 解:A.44gN2O的物质的量为:$\frac{44g}{44g/mol}$=1mol,含有的氮原子数目为2NA,故A错误;
B.不是标准状况下,不能使用标准状况下的气体摩尔体积计算22.4L氮气的物质的量,故B错误;
C.1 mol Mg变为Mg2+时失去2mol电子,失去的电子数目为2NA,故C正确;
D.没有告诉lmol•L-1K2CO3溶液的体积,无法计算溶液中含有钾离子的数目,故D错误;
故选C.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,明确标准状况下气体摩尔体积的使用条件为解答关键,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.比较乙烷、乙烯、乙炔的组成、结构和性质,不正确的叙述是( )
| A. | 这三种物质都属于气态烃 | |
| B. | 乙炔中碳的质量分数最小 | |
| C. | 溴水能与乙烯和乙炔加成,但不能与乙烷反应 | |
| D. | 一个分子中,共用电子对最多的物质是乙烷 |
15.下列化学用语的表述正确的是( )
| A. | CSO的电子式: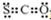 | B. | NaClO的电子式: | ||
| C. | CO2的分子示意图: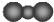 | D. | 次氯酸的结构式:H-Cl-O |
19.NA表示阿伏加德罗常数的值,下列说正确的( )
| A. | 17g氨气中所含质子数为10NA | |
| B. | 2.4g金属镁变成镁离子时失去电子数为0.1NA | |
| C. | 在标准状况下,22.4L氧气中所含的氧原子数为NA | |
| D. | 在25℃、压强为1.01×105Pa时,28g氮气所含的分子数为NA |
9.下列叙述中不正确的是( )
| A. | 一定浓度的醋酸钠溶液可使酚酞溶液变红,其原因是发生了如下反应:CH3COO-+H2O?CH3COOH+OH-,使得溶液中的c(OH-)>c(H+) | |
| B. | 在常温下,10 mL 0.2 molL-1盐酸与10 mL 0.2 molL-1 Ba(OH)2溶液充分混合,若混合后溶液的体积为20 mL,则溶液的pH=13 | |
| C. | 在0.1 molL-1 NH4Cl溶液中:c(H+)+c(NH4+)=c(Cl-) | |
| D. | 5 mL 1 molL-1 CH3COONa溶液与5 mL 1 molL-1盐酸混合液中c(Cl-)=c(Na+)>c(H+)>c(OH-) |
12.用NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 1 mol OH-中含有9NA个电子 | |
| B. | 28 g CO气体中含有NA个氧原子 | |
| C. | 1 mol/L AlCl3溶液中含有NA个Al3+ | |
| D. | 常温常压下,11.2 L甲烷气体中含有的分子数为0.5NA |
