题目内容
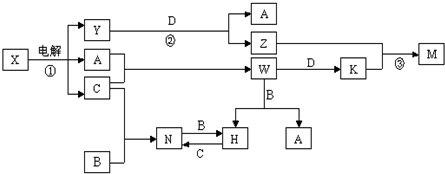
已知反应①是工业上炼铁的主要反应,A~F之间的相互转化关系如图:

(1)写出下列各物质的化学式:A ,F ;
(2)写出下列反应的化学方程式:② ;③ .

(1)写出下列各物质的化学式:A
(2)写出下列反应的化学方程式:②
考点:无机物的推断
专题:推断题
分析:反应①是工业上炼铁的主要反应,判断A为CO,固体B为Fe,和稀硫酸反应生成D为H2,浅绿色溶液E为FeSO4,气体C为CO2,通过过量石灰水生成白色沉淀F为CaCO3.
解答:
解:反应①是工业上炼铁的主要反应,判断A为CO,固体B为Fe,和稀硫酸反应生成D为H2,浅绿色溶液E为FeSO4,气体C为CO2,通过过量石灰水生成白色沉淀F为CaCO3;
(1)上述分析推断A为CO,F为CaCO3,故答案为:CO;CaCO3 ;
(2)反应②为铁和稀硫酸反应生成硫酸亚铁和氢气,反应的化学方程式为:Fe+H2SO4=FeSO4+H2↑;反应③是气体二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,反应的化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O,
故答案为:Fe+H2SO4=FeSO4+H2↑;CO2+Ca(OH)2=CaCO3↓+H2O.
(1)上述分析推断A为CO,F为CaCO3,故答案为:CO;CaCO3 ;
(2)反应②为铁和稀硫酸反应生成硫酸亚铁和氢气,反应的化学方程式为:Fe+H2SO4=FeSO4+H2↑;反应③是气体二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,反应的化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O,
故答案为:Fe+H2SO4=FeSO4+H2↑;CO2+Ca(OH)2=CaCO3↓+H2O.
点评:本题考查了物质性质的反应关系和反应现象分析判断,掌握物质性质和反应特征、工业制备原理是关键,题目较简单.

练习册系列答案
相关题目
对于可逆反应:aA(g)+bB(g)?mC(g)+nD(g);△H<0,下列说法正确的是( )
| A、浓度改变平衡必移动 |
| B、增大压强平衡必移动 |
| C、升高温度平衡必移动 |
| D、导入氦气平衡必移动 |
下列关于胶体的说法不正确的是( )
| A、可用渗析法提纯胶体 |
| B、胶体、溶液和浊液这三种分散系根本区别是分散质粒子直径的大小 |
| C、胶体微粒不能透过滤纸 |
| D、往25mL沸水中逐滴加2mL FeCl3饱和溶液,可以制得Fe(OH)3胶体 |
 (1)下列7种物质:
(1)下列7种物质: 石油是工业的血液,被誉为“黑色的金子”,是重要的能源资源和化工原料.
石油是工业的血液,被誉为“黑色的金子”,是重要的能源资源和化工原料.