题目内容
6.乙烯是重要的化工原料,工业上常以乙烯为原料合成乙酸乙酯,也可以乙烯为原料来合成聚乙烯(简称PE),合成路线如下.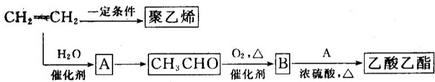
请回答下列问题:
(1)A的结构简式CH3CH2OH.B中所含的官能团结构简式-COOH.
(2)A+B→乙酸乙酯的化学方程式是CH3COOH+CH3CH2OH
 CH3COOC2H5+H2O.
CH3COOC2H5+H2O.
分析 乙烯在一定条件下发生加聚反应生成聚乙烯,聚乙烯结构简式为 ;乙烯和水发生加成反应生成乙醇,则A结构简式为CH3CH2OH,乙醇被氧化生成乙醛,乙醛被氧化生成B,B为CH3COOH,乙醇和乙酸发生酯化反应生成CH3COOCH2CH3,据此分析解答.
;乙烯和水发生加成反应生成乙醇,则A结构简式为CH3CH2OH,乙醇被氧化生成乙醛,乙醛被氧化生成B,B为CH3COOH,乙醇和乙酸发生酯化反应生成CH3COOCH2CH3,据此分析解答.
解答 解:乙烯在一定条件下发生加聚反应生成聚乙烯,聚乙烯结构简式为 ; 乙烯和水发生加成反应生成乙醇,则A结构简式为CH3CH2OH,乙醇被氧化生成乙醛,乙醛被氧化生成B,B为CH3COOH,乙醇和乙酸发生酯化反应生成CH3COOCH2CH3,
; 乙烯和水发生加成反应生成乙醇,则A结构简式为CH3CH2OH,乙醇被氧化生成乙醛,乙醛被氧化生成B,B为CH3COOH,乙醇和乙酸发生酯化反应生成CH3COOCH2CH3,
(1)通过以上分析知,A的结构简式 CH3CH2OH,B为CH3COOH,B中所含的官能团结构简式 为-COOH
,故答案为:CH3CH2OH;-COOH;
(2)在浓硫酸作催化剂条件下,乙醇和乙酸发生酯化反应生成乙酸乙酯,所以A+B→乙酸乙酯的化学方程式是CH3COOH+CH3CH2OH CH3COOC2H5+H2O,
CH3COOC2H5+H2O,
故答案为:CH3COOH+CH3CH2OH CH3COOC2H5+H2O.
CH3COOC2H5+H2O.
点评 本题考查有机物推断,为高频考点,明确官能团及其性质关系是解本题关键,熟练掌握常见有机物官能团及其性质,题目难度不大.

练习册系列答案
相关题目
16.配制250mL1mol/L的HCl溶液,需要10mol/L HCl溶液的体积为( )
| A. | 10mL | B. | 15mL | C. | 25mL | D. | 30mL |
17.一定条件下,可逆反应C(s)+CO2(g)═2CO(g)△H=+QkJ/mol,达到平衡状态,现进行如下操作:①升高反应体系的温度;②增加反应物C的用量;③缩小反应体系的体积:④减少体系中CO的量.上述措施中一定能使反应的正反应速率显著加快的( )
| A. | ①③ | B. | ①②③④ | C. | ②④ | D. | ①③④ |
14.糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质,以下叙述正确的是( )
| A. | 植物油是高分子化合物 | |
| B. | 淀粉水解的最终产物是葡萄糖 | |
| C. | 葡萄糖能发生水解和氧化反应 | |
| D. | 蛋白质溶液遇硫酸铜后产生的沉淀能重新溶于水 |
1.锂原子比镁原子少1个电子层,最外层电子数也比镁原子少1,在周期表中锂和镁的位置关系存在有“对角线”关系,“对角线”关系的元素性质存在相似性.下列关于锂的判断可能正确的是( )
| A. | Li能在空气中燃烧 | B. | Li2O只有共价键 | ||
| C. | Li2CO3能溶于水 | D. | LiOH受热不分解 |
11.下列关于钠及其化合物的叙述错误的是?( )
| A. | 取用金属钠时,所需用品至少有小刀、镊子、滤纸、玻璃片 | |
| B. | 金属钠与Ca(HCO3)2溶液反应时,既有白色沉淀又有气体逸出 | |
| C. | 生理盐水的质量分数为0.9%,与人体的血液中含量相同,它的溶质是NaCl | |
| D. | Na2O2与碱反应生成盐和水,所以Na2O2是碱性氧化物 |
15.下列四种NaHCO3溶液分别加入到四个盛有10mL 2mol•L-1盐酸的烧杯中,均加水稀释到50mL,则反应最快的是( )
| A. | 10℃20mL 3 mol•L-1的NaHCO3溶液 | B. | 20℃30mL 2 mol•L-1的NaHCO3溶液 | ||
| C. | 20℃10mL 4 mol•L-1的NaHCO3溶液 | D. | 10℃10mL 2 mol•L-1的NaHCO3溶液 |
16.关于物质的量的叙述正确的是( )
| A. | 常温常压下,4.4g CO2物质的量为0.1mol | |
| B. | 常温常压下,6.2g Na2O含有的Na+离子数为0.1mol | |
| C. | 标准状况下,1NA个H2O分子含有氧分子数为1mol | |
| D. | 标准状况下,22.4L酒精的物质的量为1mol |
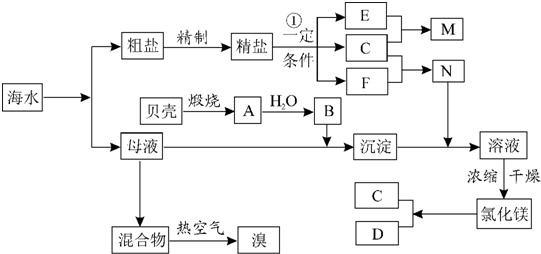
 ;
;