题目内容
11.用惰性电极电解足量的下列溶液,一段时间后停止电解,向溶液中加入一定质量的另一种物质(括号内),能使溶液完全复原的是( )| A. | CuCl2( H2O) | B. | NaOH(Na2O) | C. | CuSO4( CuO) | D. | NaCl( NaOH) |
分析 电解池中,要想使电解质溶液恢复,遵循的原则是:电解后从溶液中减少的物质是什么就利用元素守恒来加什么,据此分析.
解答 解:A.电解CuCl2溶液时一极析铜,另一极产生氯气,应再加入适量的CuCl2才能使电解质溶液与原来完全一样,故A错误;
B.电解NaOH溶液阴极2H++2e-=H2↑,阳极4OH--4e-=O2↑+2H2O,实际上被电解的是水,应加入水才能使电解质溶液与原来完全一样,故B错误;
C.电解CuSO4溶液,阴极Cu2++2e-=Cu,阳极4OH--4e-=O2↑+2H2O,加入CuO或是CuCO3,能使电解质溶液与原来完全一样,故C正确;
D.电解NaCl溶液,2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑,一极析出氯气,另一极产生氯气,应再加入适量的HCl才能使电解质溶液与原来完全一样,故D错误.
故选C.
点评 本题考查电解原理,题目难度中等,解答本题的关键是能正确判断电极反应,根据析出什么加入什么的原则判断.

练习册系列答案
相关题目
1.下面a~e是中学化学实验中常见的几种定量仪器:
(a)量筒 (b)容量瓶 (c)滴定管 (d)托盘天平 (e)温度计
(1)无“0”刻度的是ab(填写编号).
(2)下列操作能合理的是A
A.用25mL碱式滴定管量取20.00mLNaHCO3
B.用托盘天平准确称量10.20克碳酸钠固体
C.用100mL量筒量取3.2mL浓硫酸
D.用500mL容量瓶配制1mol•L-1的氢氧化钠溶液495.5mL
(3)某学生根据三次实验分别记录有关数据如下表:
请选用其中合理数据列出该氢氧化钠溶液物质的量浓度(计算结果小数点后保留4位数字):c(NaOH)=0.1044mol/L
(4)由于错误操作,使得上述所测氢氧化钠溶液的浓度偏高的是CD(填写编号).
A.中和滴定达终点时俯视滴定管内液面读数.
B.碱式滴定管用蒸馏水洗净后立即取用25.00ml待测碱溶液注入锥形瓶进行滴定.
C.酸式滴定管用蒸馏水洗净后立即装标准溶液来滴定.
D.把配好的标准溶液倒入刚用蒸馏水洗净的试剂瓶中然后用来滴定.
(a)量筒 (b)容量瓶 (c)滴定管 (d)托盘天平 (e)温度计
(1)无“0”刻度的是ab(填写编号).
(2)下列操作能合理的是A
A.用25mL碱式滴定管量取20.00mLNaHCO3
B.用托盘天平准确称量10.20克碳酸钠固体
C.用100mL量筒量取3.2mL浓硫酸
D.用500mL容量瓶配制1mol•L-1的氢氧化钠溶液495.5mL
(3)某学生根据三次实验分别记录有关数据如下表:
| 滴定次数 | 待测氢氧化钠溶液的体积(ml) | 0.1000mol?L-1盐酸的体积(ml) |
| 第一次 | 25.00 | 26.11 |
| 第二次 | 25.00 | 28.74 |
| 第三次 | 25.00 | 26.09 |
(4)由于错误操作,使得上述所测氢氧化钠溶液的浓度偏高的是CD(填写编号).
A.中和滴定达终点时俯视滴定管内液面读数.
B.碱式滴定管用蒸馏水洗净后立即取用25.00ml待测碱溶液注入锥形瓶进行滴定.
C.酸式滴定管用蒸馏水洗净后立即装标准溶液来滴定.
D.把配好的标准溶液倒入刚用蒸馏水洗净的试剂瓶中然后用来滴定.
2.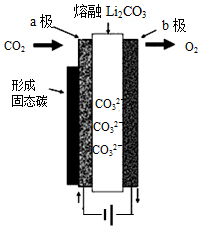 2010年乔治华盛顿大学Licht和他的合作者设计的捕获二氧化碳的电化学部分装置如图所示.下列说法正确的是( )
2010年乔治华盛顿大学Licht和他的合作者设计的捕获二氧化碳的电化学部分装置如图所示.下列说法正确的是( )
 2010年乔治华盛顿大学Licht和他的合作者设计的捕获二氧化碳的电化学部分装置如图所示.下列说法正确的是( )
2010年乔治华盛顿大学Licht和他的合作者设计的捕获二氧化碳的电化学部分装置如图所示.下列说法正确的是( )| A. | 化学能转变为电能 | |
| B. | 阴极的电极反应为:CO2+4e-=C↓+2O2- | |
| C. | 阳极的电极反应为:2CO32--4e-=2CO2↑+O2↑ | |
| D. | 阴极上每通过4mole-,阴极区有1molCO2参与反应 |
19.易形成简单阴离子的元素是( )
| A. | O | B. | Mg | C. | Na | D. | He |
6.向下列溶液中逐滴加入NaOH溶液至过量,先有白色沉淀生成,然后沉淀又消失的是( )
| A. | CuCl2溶液 | B. | AlCl3溶液 | C. | MgCl2溶液 | D. | BaCl2溶液 |
16.下列有关阿佛加德罗常数(NA)的说法错误的是( )
| A. | 0.5molH2O含有的原子数目为1.5NA | B. | 0.5molNH3含有的电子数目为4NA | ||
| C. | 28gCO含有的分子数目为NA | D. | 2NA个氯气分子的物质的量是2mol |
3.下列说法中,正确的是( )
| A. | 钠和氢气分别在氯气中燃烧,都产生白色烟雾 | |
| B. | 铜丝在氯气中燃烧,生成蓝色的氯化铜 | |
| C. | 液氯和氯水中滴入硝酸银溶液均会产生白色沉淀 | |
| D. | 新制氯水显酸性,向其中滴加少量紫色石蕊试液后溶液呈红色 |
20.在无土栽培中,需配制一定组成的植物营养液.已知某植物营养液的配方为0.6mol KCl、0.4mol K2SO4、0.20mol ZnSO4和1LH2O.若以KCl、K2SO4、ZnCl2和1LH2O为原料配得相同组成的营养液,需三种溶质的物质的量为( )
| A. | 0.20 mol、0.60 mol、0.20mol | B. | 0.30 mol、0.60 mol、0.10 mol | ||
| C. | 0.40 mol、0.60 mol、0.10 mol | D. | 0.20 mol、0.10mol、0.60 mol |