题目内容
11. 现有纯铁片、纯银片、纯铜片,稀硫酸、FeSO4 溶液、Fe2(SO4)3溶液、大烧杯、导线若干,请运用原电池原理设计实验,验证Cu2+、Fe3+的氧化性强弱.
现有纯铁片、纯银片、纯铜片,稀硫酸、FeSO4 溶液、Fe2(SO4)3溶液、大烧杯、导线若干,请运用原电池原理设计实验,验证Cu2+、Fe3+的氧化性强弱.(1)写出电极反应式,负极:Cu-2e-=Cu2+.正极:2Fe3++2e-=2Fe2+.
(2)请在如图方框中画出原电池的装置图,标出外电路电子流向(注明电极材料、电解质溶液,连成闭合回路).
(3)Cu2+、Fe3+的氧化性由强到弱的顺序为:Fe3+>Cu2+.
(4)该装置反应一段时间后,当溶液的质量增加3.2g时,通过导线的电子的物质的量是0.1mol.
分析 Fe3+氧化性比Cu2+强,可发生2Fe3++Cu=2Fe2++Cu2+,反应中Cu被氧化,为原电池的负极,则正极可为碳棒或不如Cu活泼的金属,电解质溶液为氯化铁溶液,正极发生还原反应,负极发生氧化反应,以此解答该题.
解答 解:(1)Fe3+氧化性比Cu2+强,可发生2Fe3++Cu=2Fe2++Cu2+,Cu被氧化,为原电池的负极,负极反应为Cu-2e-=Cu2+,正极Fe3+被还原,电极方程式为2Fe3++2e-=2Fe2+,故答案为:Cu-2e-=Cu2+;2Fe3++2e-=2Fe2+;
(2)Fe3+氧化性比Cu2+强,可发生2Fe3++Cu=2Fe2++Cu2+,Cu被氧化,为原电池的负极,正极Fe3+被还原,正极可为碳棒,电解质溶液为氯化铁,
则原电池装置图可设计为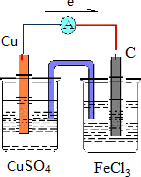 ,电子从铜极流向碳极,故答案为:
,电子从铜极流向碳极,故答案为: ;
;
(3)根据反应:2Fe3++Cu=2Fe2++Cu2+,氧化剂的氧化性强于氧化产物的氧化性,即Cu2+、Fe3+的氧化性由强到弱的顺序为Fe3+>Cu2+,故答案为:Fe3+>Cu2+;
(4)该装置反应一段时间后,当溶液的质量增加3.2g时,即消耗的金属铜质量是3.2g即0.05mol,根据负极反应Cu-2e-=Cu2+,电子转移0.1mol,故答案为:0.1mol.
点评 本题综合考查原电池的设计及原电池的工作原理,为高考常见题型,侧重于学生的分析能力和计算能力的考查,有利于培养学生的良好的科学素养,难度不大,注意从氧化还原反应的角度由电池反应判断电极反应.

练习册系列答案
相关题目
1.甲烷分子中的四个氢原子都可以被取代.若甲烷分子中的四个氢原子都被苯基取代,则可得到分子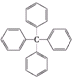 .对该分子的描述正确的是( )
.对该分子的描述正确的是( )
 .对该分子的描述正确的是( )
.对该分子的描述正确的是( )| A. | 分子式为C25H20 | B. | 其不是芳香烃 | ||
| C. | 所有碳原子都在同一平面上 | D. | 该物质为脂环烃 |
2.取等质量两种烃A、B完全燃烧,生成的CO2与消的O2的量相同,这两种烃之间的关系正确的是( )
| A. | 一定互为同分异构体 | B. | 一定互为同系物 | ||
| C. | 实验式一定相同 | D. | 只能是同种物质 |
6.元素在周期表中的位置反映了元素的原子结构和元素的性质,下列有关说法正确的是( )
| A. | 同一元素不可能既有金属性,又有非金属性 | |
| B. | 非金属元素组成的化合物中只含共价键 | |
| C. | 第三周期主族元素的最高化合价等于它所在的主族序数 | |
| D. | 短周期元素形成简单离子后,最外层电子都达到8电子稳定结构 |
20.X、Y、Z均为短周期元素,它们在周期表中的相对位置如图所示,已知X、Y、Z的质子数之和为31.试回答:
(1)它们的元素符号是C;Mg;Al.
(2)X的最高价氧化物的化学式为CO2,X元素的最简单气态氢化物的分子式为CH4.
(3)Z的最高价氧化物是两性(选填“两性”“酸性”或“碱性”)氧化物.
(4)Y与水反应的化学方程式2Mg+2H2O═Mg(OH)2+H2↑.
| X | ||
| Y | Z |
(2)X的最高价氧化物的化学式为CO2,X元素的最简单气态氢化物的分子式为CH4.
(3)Z的最高价氧化物是两性(选填“两性”“酸性”或“碱性”)氧化物.
(4)Y与水反应的化学方程式2Mg+2H2O═Mg(OH)2+H2↑.
1.甲烷和乙醇均属于( )
| A. | 酸 | B. | 碱 | C. | 氧化物 | D. | 有机物 |

 氯元素的单质及其化合物在生产生活中都很重要.回答下列问题:
氯元素的单质及其化合物在生产生活中都很重要.回答下列问题: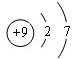 .
.