题目内容
11.将7.84LH2S和11.2LO2(均在标准状况下)的混合物放入一密闭容器中,点燃,使之反应,然后冷却到室温,经测定,反应物均无剩余,问:(1)反应后容器中氧化产物有S、SO2(填有关物质的化学式).
(2)氧化产物的总质量为多少克?(写出计算过程)
分析 7.84LH2S和11.2LO2(均在标准状况下)的物质的量分别为:n(H2S)=$\frac{7.84L}{22.4L/mol}$=0.35mol=0.35mol,n(O2)=$\frac{11.2L}{22.4L/mol}$=0.5mol,
(1)反应物均无剩余,由元素守恒可知n(H2O)=n(H2S)=0.35mol,根据O元素守恒可知生成0.35mol水消耗氧气的物质的量为:0.35mol×$\frac{1}{2}$=0.175mol,其余氧元素生成了SO2,生成SO2的物质的量为:0.5mol-0.175mol=0.325mol<0.35mol,据此可判断氧化产物组成;
(2)硫化氢与氧气的反应中的氧化产物为S、SO2,还原产物只有H2O,其中生成水的质量为:m(H2O)=0.35mol×18g/mol=6.3g,
混合气体的总质量减去生成的水的质量为容器中氧化产物的质量,据此计算出氧化产物的总质量.
解答 解:7.84LH2S和11.2LO2(均在标准状况下)的物质的量分别为:n(H2S)=$\frac{7.84L}{22.4L/mol}$=0.35mol=0.35mol,n(O2)=$\frac{11.2L}{22.4L/mol}$=0.5mol,
(1)反应物均无剩余,由元素守恒可知n(H2O)=n(H2S)=0.35mol,根据O元素守恒可知生成0.35mol水消耗氧气的物质的量为:0.35mol×$\frac{1}{2}$=0.175mol,其余氧元素生成了SO2,生成SO2的物质的量为:0.5mol-0.175mol=0.325mol<0.35mol,说明氧化产物为S、SO2 的混合物,
故答案为:S、SO2;
(2)硫化氢与氧气的反应中的氧化产物为S、SO2,还原产物只有H2O,其中生成水的质量为:m(H2O)=0.35mol×18g/mol=6.3g,
混合气体的总质量减去生成的水的质量为容器中氧化产物的质量,故容器中氧化产物的总质量为:34g/mol×0.35mol+0.5mol×32g/mol-6.3g=21.6g,
答:氧化产物的总质量为21.6g.
点评 本题考查了混合物反应的计算,题目难度中等,明确发生反应的原理为解答关键,注意掌握守恒思想在化学计算中的应用方法,试题培养了学生的分析能力及化学计算能力.

| A. | 常温下pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,水的电离程度前者比后者大 | |
| B. | 反应Hg(1)+H2SO4(aq)=HgSO4(aq)+H2(g)在常温下不能自发进行,则△H>0 | |
| C. | 将纯水加热至较高温度,K变大、pH变小、呈酸性 | |
| D. | N2(g)+3H2(g)?2NH3(g)△H<0,其他条件不变时增大氮气的浓度,正逆反应速率均增大,平衡正向移动,氢气的转化率提高 |
| A. | 在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4NA | |
| B. | 氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA | |
| C. | 常温常压下,3.2gO2和3.2gO3中所含氧原子数都是0.2NA | |
| D. | 将常温下含NA个NO2、N2O4分子的混合气体的温度降至标准状况,其体积约为22.4L |
| A. | 少量碳酸氢铵溶液与足量烧碱溶液混合加热:NH4++OH-$\stackrel{△}{→}$NH3↑+H2O | |
| B. | 氨气通入稀硫酸中:NH3+H+→NH4+ | |
| C. | 稀氨水与稀盐酸混合:NH3?H2O+H+→NH4++H2O | |
| D. | 铜片溶于稀硝酸:3Cu+8H++2NO3-→3Cu2++2NO↑+4H2O |
| A. | 二氧化氮与氧气 | B. | 一氧化氮与二氧化氮 | ||
| C. | 硝酸与一氧化氮 | D. | 硝酸与水 |
| A. | Cu (CuO),加盐酸,过滤 | B. | NaCl (I2)固体,加热升华 | ||
| C. | KNO3 (K2SO4),加BaCl2溶液,过滤 | D. | MgO (Al2O3),加烧碱溶液,过滤 |
| A. | H2O | B. | CaCl2 | C. | NH4Cl | D. | HCl |
| A. | 常温常压下,36g18O2中所含的中子数为16NA | |
| B. | 8.0g Cu2S和CuO的混合物中含有铜原子数为0.1NA | |
| C. | 电解饱和食盐水时,阳极上生成22.4L气体时转移的电子数为2NA | |
| D. | 标准状况下,2.24 LCl2溶于水中达到饱和,可得到HClO分子的数目是0.1NA |
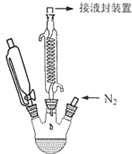 二茂铁的化学式为(C5H5)2Fe,它是一种橙黄色针状晶体,熔点173--174℃,100℃以上显著升华,沸点249℃,不溶于水,可溶于甲醇、乙醇、乙醚和苯等有机溶剂,可作高性能的火箭燃料添加剂.实验室制备二茂铁的反应原理为:8KOH+2C5H6+FeCl2•4H2O$\frac{\underline{\;\;△\;\;}}{\;}$(C5H5)2Fe+2KCl+6KOH•H2O实验装置如图所示(加热及磁力搅拌装置未画出).
二茂铁的化学式为(C5H5)2Fe,它是一种橙黄色针状晶体,熔点173--174℃,100℃以上显著升华,沸点249℃,不溶于水,可溶于甲醇、乙醇、乙醚和苯等有机溶剂,可作高性能的火箭燃料添加剂.实验室制备二茂铁的反应原理为:8KOH+2C5H6+FeCl2•4H2O$\frac{\underline{\;\;△\;\;}}{\;}$(C5H5)2Fe+2KCl+6KOH•H2O实验装置如图所示(加热及磁力搅拌装置未画出).