题目内容
11.关于元素周期表的叙述正确的是( )| A. | 元素周期表共7个横行,包含4个短周期和3个长周期 | |
| B. | 元素周期表共16个纵行,包含7个主族、7个副族、1个第Ⅷ族、1个零族 | |
| C. | 第五周期第ⅡA元素与第ⅢA元素原子序数相差11 | |
| D. | 第ⅣA族相邻元素原子序数之差可能为2、8、18、32 |
分析 A、元素周期表共7个横行,7个周期,包含3个短周期和4个长周期;
B、元素周期表共18个纵行,16个族,包含7个主族、7个副族、1个第Ⅷ族、1个零族;
C、第ⅡA族与第ⅢA族的元素,短周期相差1、4和5周期相差11、6和7周期相差25;
D、一至七周期元素的种类数为2、8、8、18、18、32、26;
解答 解:A、元素周期表共7个横行,7个周期,包含3个短周期和4个长周期,故A错误;
B、元素周期表共18个纵行,16个族,包含7个主族、7个副族、1个第Ⅷ族、1个零族,故B错误;
C.第ⅡA族与第ⅢA族的元素,原子序数之差在短周期相差1(相邻)、4和5周期相差11(中间为副族和第ⅤⅢ族)、6和7周期相差25(中间为副族和第ⅤⅢ族且含锕系和镧系),所以第五周期第ⅡA元素与第ⅢA元素原子序数相差11,故C正确;
D、一至七周期元素的种类数为2、8、8、18、18、32、26,则同主族相邻元素原子序数之差可以是2、8、18、32,而第ⅣA族相邻元素原子序数之差不可能为2,故D错误;
故选C.
点评 本题考查元素周期表的结构及应用,为高频考点,把握元素在周期表的位置、元素的性质及元素周期律为解答的关键,注意整体把握周期表的结构,题目难度不大.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
6.关于168O,说法正确的是( )
| A. | 属于第二周期第VIA族元素 | B. | 原子最外层电子数为8 | ||
| C. | 质子数为16 | D. | 与167N互为同位素 |
3. 有A、B、C、D、E五种元素,其相关信息如表:
有A、B、C、D、E五种元素,其相关信息如表:
请回答下列问题:
(1)写出E元素原子基态时的电子排布式1s22s22p63s23p63d104s1.
(2)C元素的第一电离能比氧元素的第一电离能大(填“大”或“小”).
(3)CA3分子中C原子的杂化类型是sp3.
(4)A、C、E三种元素可形成[E(CA3)4]2+,其中存在的化学键类型有①③(填序号);
①配位键 ②金属键 ③极性共价键 ④非极性共价键 ⑤离子键 ⑥氢键
若[E(CA3)4]2+具有对称的空间构型,且当[E(CA3)4]2+中的两个CA3被两个Cl-取代时,能得到两种不同结构的产物,则[E(CA3)4]2+的空间构型为a(填序号).
a.平面正方形 b.正四面体 c.三角锥形 d.V形
(5)B与D可形成离子化合物,其晶胞结构如图所示.其中D离子的配位数为8,若该晶体的密度为a g•cm-3,则该晶胞的体积是$\frac{\frac{78}{{N}_{A}}×4}{a}$ cm3(写出表达式即可).
 有A、B、C、D、E五种元素,其相关信息如表:
有A、B、C、D、E五种元素,其相关信息如表:| 元素 | 相关信息 |
| A | A原子的1s轨道上只有1个电子 |
| B | B是电负性最大的元素 |
| C | C基态原子的2p轨道中有3个未成对电子 |
| D | D是主族元素且与E同周期,其最外能层 上有2个运动状态不同的电子 |
| E | E能形成红色(或砖红色)的E2O和黑色的EO两种氧化物 |
(1)写出E元素原子基态时的电子排布式1s22s22p63s23p63d104s1.
(2)C元素的第一电离能比氧元素的第一电离能大(填“大”或“小”).
(3)CA3分子中C原子的杂化类型是sp3.
(4)A、C、E三种元素可形成[E(CA3)4]2+,其中存在的化学键类型有①③(填序号);
①配位键 ②金属键 ③极性共价键 ④非极性共价键 ⑤离子键 ⑥氢键
若[E(CA3)4]2+具有对称的空间构型,且当[E(CA3)4]2+中的两个CA3被两个Cl-取代时,能得到两种不同结构的产物,则[E(CA3)4]2+的空间构型为a(填序号).
a.平面正方形 b.正四面体 c.三角锥形 d.V形
(5)B与D可形成离子化合物,其晶胞结构如图所示.其中D离子的配位数为8,若该晶体的密度为a g•cm-3,则该晶胞的体积是$\frac{\frac{78}{{N}_{A}}×4}{a}$ cm3(写出表达式即可).
20.下列物质中,能与醋酸发生反应的是( )
①石蕊 ②乙醇 ③氢氧化铜 ④金属铝 ⑤氧化镁 ⑥碳酸钙.
①石蕊 ②乙醇 ③氢氧化铜 ④金属铝 ⑤氧化镁 ⑥碳酸钙.
| A. | ①③④⑤⑥⑦ | B. | ②③④⑤ | C. | ①②④⑤⑥ | D. | 全部 |
1.硅作为一种新型能源被广泛开发利用,关于其有利因素的下列说法中,你认为不正确的是( )
| A. | 硅燃烧产物对环境产生的污染,容易得到有效控制 | |
| B. | 硅燃烧可以放出较多的热量 | |
| C. | 自然界中硅的贮存量丰富,可以从自然界直接获得单质硅 | |
| D. | 硅便于运输、贮存,从安全角度考虑,硅是最佳的燃料之一 |
11.常温下,物质的量浓度相等的下列溶液pH由大到小的顺序是( )
①Na2CO3②CH3COONa ③CH3CH2ONa ④NH4NO3⑤NaHSO4⑥苯酚钠 ⑦NaHCO3.
①Na2CO3②CH3COONa ③CH3CH2ONa ④NH4NO3⑤NaHSO4⑥苯酚钠 ⑦NaHCO3.
| A. | ③①⑥⑦②④⑤ | B. | ⑥①②⑦③④⑤ | C. | ⑤④③①⑥⑦② | D. | ⑥③⑦①②④⑤ |
12.如图有关于化学反应速率和化学平衡的四个图象,下列反应中全部符合上述图象的反应是( )
| A. | 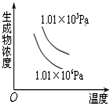 4NH3(g)+5O2(g)?4NO+6H2O(g);△H=-Q1kJ/mol(Q1>0) | |
| B. | 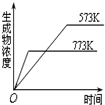 2SO3(g)?2SO2(g)+O2(g);△H=+Q2 kJ/mol(Q2>0) | |
| C. |  N2(g)+3H2(g)?2NH3(g);△H=-Q3kJ/mol(Q3>0) | |
| D. | 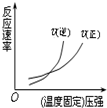 H2(g)+CO(g)?C(s)+H2O(g);△H=+Q4kJ/mol(Q4>0) |
 .
. .
. 短周期元素a、b、c、d的原子序数依次增大.它们分属于不同主族,这四种元素的原子电子层数之和为8.A、B、C、D依次为a、b、c、d的单质,甲、乙、丙分子内原子数依次为4、3、2.在一定条件下可以发生如图所示的化合反应.
短周期元素a、b、c、d的原子序数依次增大.它们分属于不同主族,这四种元素的原子电子层数之和为8.A、B、C、D依次为a、b、c、d的单质,甲、乙、丙分子内原子数依次为4、3、2.在一定条件下可以发生如图所示的化合反应. ,若将甲通入乙中所得溶液PH大于7,用方程式表示溶液PH大于7 的原因:NH3•H2O?NH4++OH-.
,若将甲通入乙中所得溶液PH大于7,用方程式表示溶液PH大于7 的原因:NH3•H2O?NH4++OH-.