题目内容
20.两种气态烃组成的混合气体0.1mol,完全燃烧得0.18mol CO2和3.6g H2O,下列关于该混合气体的说法正确的是( )| A. | 一定有乙烯 | B. | 一定没有乙烯 | C. | 一定有甲烷 | D. | 一定有乙烷 |
分析 3.6g水的物质的量为$\frac{3.6g}{18g/mol}$=0.2mol,即0.1mol混合烃完全燃烧生成0.18molCO2和0.2molH2O,根据元素守恒,则混合烃的平均分子式为C1.8H4,而烃类中碳原子数小于1的只有甲烷,判断混合气体中一定含有甲烷,则另一种烃中一定含有4个H原子,结合各选项进行判断.
解答 解:3.6g水的物质的量为$\frac{3.6g}{18g/mol}$=0.2mol,即0.1mol混合烃完全燃烧生成0.18molCO2和0.2molH2O,根据元素守恒,则混合烃的平均分子式为C1.8H4,而烃类中碳原子数小于1的只有甲烷,判断混合气体中一定含有甲烷,则另一种烃中一定含有4个H原子,可能为乙烯、丙炔,一定不可能为乙烷,故ABD错误,C正确,
故选C.
点评 本题考查了有机物分子式的计算,题目难度中等,注意掌握利用平均分子组成判断烃的组成的方法,常用方法有:平均碳法、平均氢法、平均碳氢分子式法、平均式量法等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
15.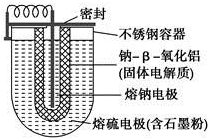 如图所示,NaS电池是当前开发的一种高性能可充电电池,它所贮存的能量为常用铅蓄电池的5倍(按相同质量计),电池反应为
如图所示,NaS电池是当前开发的一种高性能可充电电池,它所贮存的能量为常用铅蓄电池的5倍(按相同质量计),电池反应为
2Na(l)+S8(l)$?_{放电}^{充电}$Na2Sn.下列说法不正确的是( )
 如图所示,NaS电池是当前开发的一种高性能可充电电池,它所贮存的能量为常用铅蓄电池的5倍(按相同质量计),电池反应为
如图所示,NaS电池是当前开发的一种高性能可充电电池,它所贮存的能量为常用铅蓄电池的5倍(按相同质量计),电池反应为2Na(l)+S8(l)$?_{放电}^{充电}$Na2Sn.下列说法不正确的是( )
| A. | 外室熔融硫中添加石墨粉主要是为了增强导电性 | |
| B. | 放电时Na+向正极移动 | |
| C. | 充电时阳极反应式为8S-16e-═nS8 | |
| D. | 充电时钠极与外接电源的正极相连 |
5.下列物质中,属于混合物的是( )
| A. | 酒精 | B. | 碘酒 | C. | 水银 | D. | 黄金 |
12.下列物质属于纯净物的是( )
| A. | 氯乙烯 | B. | 汽油 | C. | 牛奶 | D. | 聚乙烯 |
9.由A、B两种气态烃组成的混合气体,对H2 的相对密度为17,常温常压下,取这两种混合气体10ml与80ml氧气(过量)混合,当完全燃烧后恢复到原状态时,测得气体的体积为70ml,则两种气态烃的可能组成为( )
| A. | CH4和C2H4 | B. | C2H4和C3H4 | C. | C2H4和C2H6 | D. | C3H6和C2H4 |
10.下列有关物质的性质和该性质的应用均正确的是( )
| A. | SO2具有氧化性,用来杀菌消毒 | |
| B. | 氢氟酸具有强酸性,用氢氟酸蚀刻玻璃 | |
| C. | 碳酸氢钠热稳定性弱,用作焙制糕点的发酵粉 | |
| D. | 铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸 |

 .
. .
.