题目内容
5.设NA表示阿伏加德罗常数,下列叙述中正确的是( )| A. | 标准状况下,22.4L乙醇含有的分子数为 NA | |
| B. | 1.8g的NH4+离子中含有的电子数为NA | |
| C. | 在含1mol氢氧化铁的胶体中,胶粒数目为NA | |
| D. | 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl- 个数为NA |
分析 A、标况下乙醇为液态;
B、求出铵根离子的物质的量,然后根据1mol铵根离子中含10个电子;
C、一个氢氧化铁胶粒是多个氢氧化铁的聚集体;
D、溶液体积不明确.
解答 解:A、标况下乙醇为液态,故不能根据气体摩尔体积来计算其物质的量和分子个数,故A错误;
B、1.8g铵根离子的物质的量为0.1mol,而1mol铵根离子中含10个电子,故0.1mol铵根离子中含NA个电子,故B正确;
C、一个氢氧化铁胶粒是多个氢氧化铁的聚集体,故1mol氢氧化铁形成的胶粒的个数小于NA个,故C错误;
D、溶液体积不明确,故溶液中的氯离子的个数无法计算,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
15.如图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )
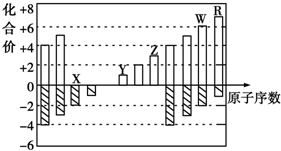

| A. | 离子半径:Y>Z>X | |
| B. | 气态氢化物的稳定性:R<W | |
| C. | WX3和水反应形成的化合物是离子化合物 | |
| D. | Y和Z两者最高价氧化物对应的水化物能相互反应 |
13.下列说法正确的是( )
| A. | 最外层有4个电子的原子都是非金属原子 | |
| B. | 同一主族的两种元素的原子序数之差不可能是44 | |
| C. | COCl2分子和CCl4分子中所有原子都满足最外层8电子结构 | |
| D. | 同主族金属的原子,半径越大,熔点越高 |
20.下列关于物质分类的说法正确的是( )
| A. | CO2、NO2均为酸性氧化物 | B. | 石英、水玻璃均为纯净物 | ||
| C. | NaCl、BaSO4均为强电解质 | D. | 烧碱、纯碱均为碱 |
10.胶状液氢(主要成分是H2和CH4)有望用于未来的运载火箭和空间运输系统.实验测得:101kPa时,H2的燃烧热为285.8kJ•mol-1,CH4的燃烧热为890.3kJ•mol-1.下列热化学方程式书写正确的是( )
| A. | CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | $\frac{1}{2}$CH4(g)+O2(g)═$\frac{1}{2}$CO2(g)+H2O(l)△H=-445.15 kJ•mol-1 | |
| C. | CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.3 kJ | |
| D. | 2H2(g)+O2(g)═2H2O(l)△H=-285.8 kJ•mol-1 |
17.常温下,向等物质的量浓度的两种一元酸的钠盐溶液中,分别通入少量的二氧化碳气体,发生如下反应:NaA+CO2+H2O═NaHCO3+HA;2NaB+CO2+H2O═Na2CO3+2HB;则等物质的量浓度的HA和HB在水中电离出H+的能力大小关系是( )
| A. | HA较强 | B. | HB较强 | C. | 两者一样 | D. | 无法比较 |
14.同周期的A、B、D三种元素,其最高价氧化物对应水化物的酸性强弱顺序是HAO4>H2BO4>H3DO4,则下列判断错误的是( )
| A. | 气态氢化物稳定性HA>H2B>DH3 | B. | 原子半径A>B>D | ||
| C. | 非金属性A>B>D | D. | 阴离子还原性B2->A- |
15.多晶硅是太阳能光伏产业的基础材料.制备多晶硅必须先得到高纯硅.三氯甲硅烷(SiHCl3)是一种可燃,易与水反应的气体,当前制备高纯硅的主要方法是在一定条件下以三氯甲硅烷为原料用氢气还原,其生产流程如图所示:

(1)①流化床反应器中主要反应的化学方程式是Si+3HCl$\frac{\underline{\;高温\;}}{\;}$SiHCl3+H2,
在生成的产物中,SiHCl3大约占85%,还有SiCl4、SiH2Cl2、SiH3Cl等,提纯SiHCl3的主要工艺操作依次是沉降、冷凝和精馏.
②整个制备过程中必须保证无水无氧.SiHCl3遇H2O剧烈反应生成H2SiO3、HCl和另一种物质,写出该反应的化学方程式:SiHCl3+3H2O═H2SiO3↓+3HCl↑+H2↑.
③H2还原SiHCl3过程中若混入O2,可能引起的后果是O2与SiHCl3、H2混合可能引起爆炸.
(2)该工艺流程可循环利用的物质是H2和HCl.
(3)Na2SiO3的水溶液俗称水玻璃,用水玻璃可制得高纯度SiO2.取少量水玻璃于试管中,逐滴加入饱和NH4Cl溶液,振荡.观察到的实验现象是试管中有白色胶状沉淀生成,有刺激性气味气体生成.
(4)电弧炉中制得的粗硅中含有副产物SiC,已知其中Si和SiC的物质的量之比为2:1,
制取粗硅时的化学方程式是3SiO2+7C═2Si+SiC+6CO↑,
若在反应中生成了2.8g Si,则转移电子数为0.6NA或3.612×1023.

| 物质 | Si | SiCl4 | SiHCl3 | SiH2Cl2 | SiH3Cl | HCl | SiH4 |
| 沸点/℃ | 2 355 | 57.6 | 31.8 | 8.2 | -30.4 | -84.9 | -111.9 |
在生成的产物中,SiHCl3大约占85%,还有SiCl4、SiH2Cl2、SiH3Cl等,提纯SiHCl3的主要工艺操作依次是沉降、冷凝和精馏.
②整个制备过程中必须保证无水无氧.SiHCl3遇H2O剧烈反应生成H2SiO3、HCl和另一种物质,写出该反应的化学方程式:SiHCl3+3H2O═H2SiO3↓+3HCl↑+H2↑.
③H2还原SiHCl3过程中若混入O2,可能引起的后果是O2与SiHCl3、H2混合可能引起爆炸.
(2)该工艺流程可循环利用的物质是H2和HCl.
(3)Na2SiO3的水溶液俗称水玻璃,用水玻璃可制得高纯度SiO2.取少量水玻璃于试管中,逐滴加入饱和NH4Cl溶液,振荡.观察到的实验现象是试管中有白色胶状沉淀生成,有刺激性气味气体生成.
(4)电弧炉中制得的粗硅中含有副产物SiC,已知其中Si和SiC的物质的量之比为2:1,
制取粗硅时的化学方程式是3SiO2+7C═2Si+SiC+6CO↑,
若在反应中生成了2.8g Si,则转移电子数为0.6NA或3.612×1023.
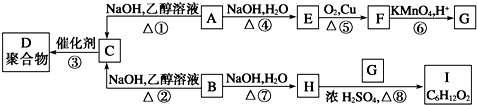
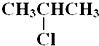 .
.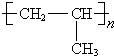 .
.