题目内容
下列实验装置图及实验用品均正确的是(部分夹持仪器未画出)( )
A、 实验室用乙醇制取乙烯 |
B、 实验室制取乙酸乙酯 |
C、 石油分馏 |
D、 实验室制取硝基苯 |
考点:化学实验方案的评价
专题:
分析:A.在170℃时制备乙烯;
B.反应生成乙酸乙酯,饱和碳酸钠可除去乙酸、乙醇,降低乙酸乙酯的溶解度;
C.分馏时测定馏分的温度;
D.水浴加热至50~60℃可制备硝基苯.
B.反应生成乙酸乙酯,饱和碳酸钠可除去乙酸、乙醇,降低乙酸乙酯的溶解度;
C.分馏时测定馏分的温度;
D.水浴加热至50~60℃可制备硝基苯.
解答:
解:A.在170℃时制备乙烯,则温度计的水银球应在反应液面以下,故A错误;
B.反应生成乙酸乙酯,饱和碳酸钠可除去乙酸、乙醇,降低乙酸乙酯的溶解度,图中制备实验合理,故B正确;
C.分馏时测定馏分的温度,则温度计的水银球应在蒸馏烧瓶的支管口处,故C错误;
D.水浴加热至50~60℃可制备硝基苯,图中温度控制不合理,故D错误;
故选B.
B.反应生成乙酸乙酯,饱和碳酸钠可除去乙酸、乙醇,降低乙酸乙酯的溶解度,图中制备实验合理,故B正确;
C.分馏时测定馏分的温度,则温度计的水银球应在蒸馏烧瓶的支管口处,故C错误;
D.水浴加热至50~60℃可制备硝基苯,图中温度控制不合理,故D错误;
故选B.
点评:本题考查化学实验方案的评价,为高频考点,把握物质的制备、混合物分馏提纯及实验装置的作用等为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案
相关题目
下列说法不正确的是( )
A、
| ||||
B、
| ||||
| C、常温常压下,只有一种元素的单质是液态 | ||||
| D、常温常压下,气态单质的分子都是由非金属元素的原子形成的 |
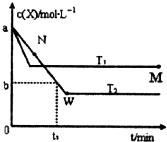 在恒容密闭容器中通入一定量的X气体与Y气体并发生反应:2X(g)+Y(g)?2Z(g),测得在温度T1、T2下X的物质的量浓度c(x)随时间t变化的曲线如图所示,下列叙述正确的是( )
在恒容密闭容器中通入一定量的X气体与Y气体并发生反应:2X(g)+Y(g)?2Z(g),测得在温度T1、T2下X的物质的量浓度c(x)随时间t变化的曲线如图所示,下列叙述正确的是( )| A、该反应进行到M点放出的热量大于进行到W点放出的热量 | ||
B、T2下,在0?t1时间内,υ(Y)=
| ||
| C、M点的平衡常数比W点的平衡常数小 | ||
| D、M点时再加入一定量的X,平衡后X的转化率增大 |
初步提纯下列物质(括号内为少量杂质),选用的试剂和分离方法均正确的是( )
| 序号 | 物质 | 试剂 | 分离方法 |
| ① | 乙酸乙酯(乙酸) | NaOH溶液 | 分液 |
| ② | 乙烷(乙烯) | 氢气 | 洗气 |
| ③ | 乙醇(水) | 生石灰 | 蒸馏 |
| ④ | 苯(环己烷) | 水 | 分液 |
| A、①② | B、①③ | C、③ | D、④③ |
下列说法不正确的是( )
| A、等物质的量浓度的 NH4HSO4溶液和NaOH溶液等体积混合,溶液中各离子浓度大小关系为:c(Na+)=c(SO42-)>c(NH4+)>c(H+)>c(OH-) | ||
B、25℃时,将a mo1?L-l氨水与0.01 moI?L-1盐酸等体积混合,反应完全时溶液中c(NH4+)=c(C1-),用含a的代数式表示NH3?H2O的电离常数Kb=
| ||
C、 某温度下,相同体积、相同pH的盐酸和醋酸溶液分别加水稀释,pH随溶液体积V变化的曲线如图所示.Ⅱ为醋酸稀释时pH的变化曲线,且a、b两点水的电离程度:a<b 某温度下,相同体积、相同pH的盐酸和醋酸溶液分别加水稀释,pH随溶液体积V变化的曲线如图所示.Ⅱ为醋酸稀释时pH的变化曲线,且a、b两点水的电离程度:a<b | ||
| D、已知298K时氢氰酸(HCN)的Ka=4.9×10-10、碳酸的Ka1=4.4×10-7,Ka2=4.7×10-11,据此可推测将氢氰酸加入到碳酸钠溶液中能观察到有气泡产生 |
下列物质中,不能使酸性KMnO4溶液褪色的物质是( )
① ②乙烯 ③CH3COOH
②乙烯 ③CH3COOH
④CH3CH2OH ⑤CH2═CH-COOH ⑥
①
 ②乙烯 ③CH3COOH
②乙烯 ③CH3COOH④CH3CH2OH ⑤CH2═CH-COOH ⑥

| A、①⑤ | B、①②④⑥ |
| C、①④ | D、①③⑥ |