题目内容
有A、B、C、D四种短周期元素,A、B、C为同一周期依次相邻的3种元素,A和C的原子序数之比为3:4,且A、B、C分别与D形成三种化合物分子所含的电子数相等,请回答:
(1)X、Y、Z、W都是由上述元素中的两种组成的化合物,若X分子的空间构型为三角锥型,则X的电子式为 ;已知Y被称为绿色氧化剂,Z与Y具有相同的电子数,两者在液态时常一起作为火箭推进器的燃料,且已知0.8gZ与Y作为火箭推进剂时,能放出20.44KJ的能量(产物均为气态),请写出该反应的热化学方程式: W是中学化学中常见的物质,其分子的空间构型为直线型,且所含有的原子数多于2个,其可能的化学式为 、 (只要写出2个).
(2)甲、乙、丙都是由上述元素中的三种组成的物质,甲为食品中常见的天然高分子化合物,表示其组成的化学式为 ;乙属于无机盐类,其水溶液明显显酸性,则乙的化学式为 ;丙与甲的组成元素相同,丙的溶液呈弱酸性,其式量小于80,且其中A的质量分数为
,则丙的结构简式为 .
(1)X、Y、Z、W都是由上述元素中的两种组成的化合物,若X分子的空间构型为三角锥型,则X的电子式为
(2)甲、乙、丙都是由上述元素中的三种组成的物质,甲为食品中常见的天然高分子化合物,表示其组成的化学式为
| 6 |
| 19 |
考点:位置结构性质的相互关系应用
专题:有机物的化学性质及推断
分析:A、B、C位于同一周期相邻位置,A、C的原子序数之比为3:4,设A的原子序数为x,则C的原子序数为:x+2,则x:(x+2)=3:4,解得:x=6,则A为C元素、C为O元素、B应为N元素;
A、B、C分别与D形成化合物分子中都含有10个电子,D为H元素,据此进行解答.
A、B、C分别与D形成化合物分子中都含有10个电子,D为H元素,据此进行解答.
解答:
解:A、B、C位于同一周期相邻位置,A、C的原子序数之比为3:4,设A的原子序数为x,则C的原子序数为:x+2,则x:(x+2)=3:4,解得:x=6,则A为C元素、C为O元素、B应为N元素;A、B、C分别与D形成化合物分子中都含有10个电子,D为H元素,
(1)氨气分子的空间构型为三角锥形,则X为氨气,氨气为共价化合物,氨气的电子式为: ;
;
已知Y被称为绿色氧化剂,则Y为双氧水,Z与Y具有相同的电子数,两者在液态时常一起作为火箭推进器的燃料,则Z为N2H4,已知0.8gZ与Y作为火箭推进剂时,能放出20.44kJ的能量(产物均为气态),则32gN2H4完全燃烧放出的热量为:20.44kJ×
=817.6kJ,该反应的热化学方程式为:N2H4(l)+2H2O2(l)═N2(g)+4H2O(g);△H=-817.6KJ/mol;
W是中学化学中常见的物质,其分子的空间构型为直线型,且所含有的原子数多于2个,满足条件的物质有:CO2、C2H2、N2O,
故答案为: ;N2H4(l)+2H2O2(l)═N2(g)+4H2O(g);△H=-817.6KJ/mol;CO2、C2H2(或N2O);
;N2H4(l)+2H2O2(l)═N2(g)+4H2O(g);△H=-817.6KJ/mol;CO2、C2H2(或N2O);
(2)甲、乙、丙都是由上述元素中的三种组成的物质,甲为食品中常见的天然高分子化合物,则甲为淀粉,表示其组成的化学式为:(C6H10O5)n;
乙属于无机盐类,其水溶液明显显酸性,乙为硝酸铵,铵根离子水解溶液显示酸性,则乙的化学式为:NH4NO3;
丙与甲的组成元素相同,丙中含有C、H、O元素,丙的溶液呈弱酸性,且丙中其式量小于80,则丙中含有羧基:-COOH,且其中A的质量分数为
,则丙中含有的C原子数<
≈2.1,由于甲酸中C的质量分数为:
=
,则丙中含有2个C原子,其式量为:
=76,丙分子中中应该还含有1个羟基,所以丙的结构简式为: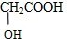 ,
,
故答案为:(C6H10O5)n;NH4NO3;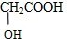 .
.
(1)氨气分子的空间构型为三角锥形,则X为氨气,氨气为共价化合物,氨气的电子式为:
 ;
;已知Y被称为绿色氧化剂,则Y为双氧水,Z与Y具有相同的电子数,两者在液态时常一起作为火箭推进器的燃料,则Z为N2H4,已知0.8gZ与Y作为火箭推进剂时,能放出20.44kJ的能量(产物均为气态),则32gN2H4完全燃烧放出的热量为:20.44kJ×
| 32g |
| 0.8g |
W是中学化学中常见的物质,其分子的空间构型为直线型,且所含有的原子数多于2个,满足条件的物质有:CO2、C2H2、N2O,
故答案为:
 ;N2H4(l)+2H2O2(l)═N2(g)+4H2O(g);△H=-817.6KJ/mol;CO2、C2H2(或N2O);
;N2H4(l)+2H2O2(l)═N2(g)+4H2O(g);△H=-817.6KJ/mol;CO2、C2H2(或N2O);(2)甲、乙、丙都是由上述元素中的三种组成的物质,甲为食品中常见的天然高分子化合物,则甲为淀粉,表示其组成的化学式为:(C6H10O5)n;
乙属于无机盐类,其水溶液明显显酸性,乙为硝酸铵,铵根离子水解溶液显示酸性,则乙的化学式为:NH4NO3;
丙与甲的组成元素相同,丙中含有C、H、O元素,丙的溶液呈弱酸性,且丙中其式量小于80,则丙中含有羧基:-COOH,且其中A的质量分数为
| 6 |
| 19 |
80×
| ||
| 12 |
| 12 |
| 46 |
| 6 |
| 23 |
| 12×2 | ||
|
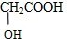 ,
,故答案为:(C6H10O5)n;NH4NO3;
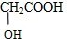 .
.
点评:本题考查了位置、结构与性质关系的综合应用,题目难度中等,正确推断各元素名称为解答根据,试题知识点较多、综合性较强,注意掌握确定有机物分子式、结构简式的方法,明确热化学方程式的书写方法.

练习册系列答案
相关题目
下列离子方程式书写正确的是( )
| A、在碘化亚铁溶液中通入足量氯气:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl- | ||||
B、用铜电极电解氯化钠饱和溶液:2Cl-+2H2O
| ||||
| C、向硫酸亚铁溶液中通入H2S气体:Fe2++H2S=FeS↓+2H+ | ||||
| D、硫酸亚铁酸性溶液中加入过氧化氢:4Fe2++2H2O2+4H+=4Fe3++4H2O |

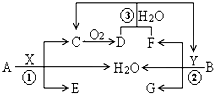 已知两种常见金属A、B分别与两种酸X、Y发生反应各生成三种产物,其转化关系如图所示,其中D为红棕色气体,G溶液呈蓝色.
已知两种常见金属A、B分别与两种酸X、Y发生反应各生成三种产物,其转化关系如图所示,其中D为红棕色气体,G溶液呈蓝色.