题目内容
6.实验室现需配制物质的量浓度为1mol•L-1的NaOH溶液480mL.(1)实验过程中用到的玻璃仪器有:烧杯、量筒、胶头滴管、500mL容量瓶、玻璃棒.
(2)要配制此溶液,需要称量NaOH固体的质量为20g.
(3)配制好的NaOH溶液不能用带磨口玻璃塞的试剂瓶存放,请解释原因SiO2+2NaOH=Na2SiO3+H2O(用化学方程式表示)
分析 (1)在烧杯中溶解、冷却后转移到容量瓶中定容,以此分析需要的仪器;
(3)结合m=nM、n=cV计算;
(3)二氧化硅与NaOH反应生成具有粘合性的硅酸钠溶液,不能用带磨口玻璃塞的试剂瓶存放.
解答 解:(1)配制480mL溶液时称量、溶解、转移、定容需要烧杯、量筒、胶头滴管、500 mL容量瓶、玻璃棒,故答案为:500 mL容量瓶;玻璃棒;
(2)需要称量NaOH固体的质量为0.5L×1mol/L×40g/mol=20g,故答案为:20g;
(3)NaOH溶液不能用带磨口玻璃塞的试剂瓶存放的原因为SiO2+2NaOH=Na2SiO3+H2O,故答案为:SiO2+2NaOH=Na2SiO3+H2O.
点评 本题考查配制一定浓度的溶液,为高频考点,把握配制溶液的步骤、仪器及试剂的保存为解答的关键,侧重分析与应用能力的考查,注意容量瓶的选择,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案
相关题目
17.下列说法中正确的是( )
| A. | 吸热反应在不加热的条件下一定不能发生 | |
| B. | 放热反应在常温下一定很容易发生 | |
| C. | 由“100KPa时石墨转化为金刚石,要吸收1.895kJ的热能”可知在100KPa压强下石墨比金刚石稳定 | |
| D. | 化学反应中的能量变化,只表现为热能的变化 |
14.在测定某温度下1mol氢气的体积实验中,实验温度下,氢气的气体摩尔体积为24.5升,实验时称取镁带的质量要控制在0.100~0.110g之间,Mg与盐酸反应,液体量瓶的量程范围是( )
| A. | 100ml~120ml | B. | 100ml~120ml | C. | 110ml~130ml | D. | 100ml~130ml |
1.除去括号中的杂质,填写涉及的离子反应方程式或化学方程式.
| 编号 | 混合物 | 方程式 |
| ① | 溶液:FeCl2 (FeCl3) | |
| ② | 固体:SiO2 (CaCO3) | |
| ③ | 气体:CO2 (HCl) | |
| ④ | 固体:NaCl(NH4Cl) |
11.金属单质与足量Cl2反应后,生成物的化学式中,不正确的是( )
| A. | FeCl2 | B. | NaCl | C. | FeCl3 | D. | CuCl2 |
18.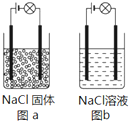 某化学兴趣小组在家中进行化学实验,按照图a连接好线路发现灯泡不亮,按照图b连接好线路发现灯泡亮,由此得出的结论正确的是( )
某化学兴趣小组在家中进行化学实验,按照图a连接好线路发现灯泡不亮,按照图b连接好线路发现灯泡亮,由此得出的结论正确的是( )
 某化学兴趣小组在家中进行化学实验,按照图a连接好线路发现灯泡不亮,按照图b连接好线路发现灯泡亮,由此得出的结论正确的是( )
某化学兴趣小组在家中进行化学实验,按照图a连接好线路发现灯泡不亮,按照图b连接好线路发现灯泡亮,由此得出的结论正确的是( )| A. | NaCl是非电解质 | |
| B. | NaCl溶液是电解质 | |
| C. | NaCl在在电流作用下电离成Na+和Cl- | |
| D. | NaCl溶液中存在大量可自由移动的离子 |
16.NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 在同温同压时,相同体积的任何气体单质所含的分子数目相同 | |
| B. | 2g氢气所含原子数目为NA | |
| C. | 在常温常压下,11.2L氮气所含的原子数目为NA | |
| D. | 17g氨气所含氢原子数目为NA |
 有机物X的键线式为:
有机物X的键线式为: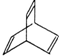
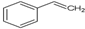
 .
.