题目内容
7.汽车尾气是城市的主要空气污染物,研究控制汽车尾气成为保护环境的首要任务.(1)汽车内燃机工作时发生反应:N2(g)+O2(g)?2NO(g),是导致汽车尾气中含有NO的原因之一.T℃时,向5L密闭容器中充入6.5molN2和7.5molO2,在5min时反应达到平衡状态,此时容器中NO的物质的量是5mol.
①5min内该反应的平均速率υ (NO)=0.2mol/(L.min);在T℃时,该反应的平衡常数K=1.25
②反应开始至达到平衡的过程中,容器中下列各项发生变化的是cd(填序号).
a.混合气体的密度 b.混合气体的压强
c.正反应速率 d.单位时间内,N2和NO的消耗量之比
(2)H2或CO可以催化还原NO以达到消除污染的目的.
已知:N2(g)+O2(g)=2NO(g)△H=+180.5kJ•mol-1
2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ•mol-1
则H2(g)与NO(g)反应生成N2(g)和H2O(l)的热化学方程式是:2H2(g)+2NO(g)=N2(g)+2H2O(l)△H=-752.1 kJ•mol-1
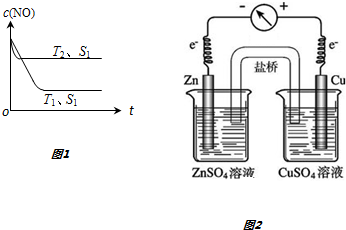
(3)当质量一定时,增大固体催化剂的表面积可提高化学反应速率.图1表示在其他条件不变时,反应:
2NO(g)+2CO(g)?2CO2(g)+N2(g) 中c(NO)随温度(T)、催化剂表面积(S)和时间(t)的变化曲线.该反应的△H<0 (填“>”或“<”).
(4)图2所示原电池的叙述,正确的是(盐桥中装有含琼胶的KCl饱和溶液)ACD
A.电子由锌片沿导线到铜片上
B.取出盐桥后,电流计依然发生偏转
C.反应中,盐桥中K+会移向CuSO4溶液
D.反应后铜片质量增加.
分析 (1)①根据v=$\frac{\frac{△n}{V}}{△t}$计算v(NO);计算平衡时各组分物质的量浓度,再根据K=$\frac{{c}^{2}(NO)}{c({N}_{2})×c({O}_{2})}$计算;
化学平衡常数是指:一定温度下,可逆反应到达平衡时,生成物的浓度系数次幂之积与反应物的浓度系数次幂之积的比,固体、纯液体不需要在化学平衡常数中写出;
②a.混合气体总质量不变,容器容积不变,混合气体的密度始终不变;
b.随反应进行混合气体总物质的量不变,恒温恒容下,压强之比等于物质的量之比;
c.随反应进行反应物浓度减小;
d.平衡之前,正反应速率大于逆反应速率,随反应进行,正反应速率减小,逆反应速率增大;
(2)已知:①N2(g)+O2(g)=2NO(g)△H=+180.5kJ•mol-1
②2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ•mol-1
根据盖斯定律,②-①可得:2H2(g)+2NO(g)=N2(g)+2H2O(l);
(3)温度越高反应速率越快,到达平衡时间越短,故温度T2>T1,升高温度NO的浓度增大,说明平衡逆向移动,则正反应为放热反应;
(4)A.Zn为负极,Cu为正极,电子由负极沿导线移向正极;
B.取出盐桥后,处于断路状态,不能形成原电池;
C.反应中,盐桥中K+会移向正极;
D.Cu为正极,发生还原反应,析出Cu.
解答 解:(1)①5min时反应达到平衡状态,容器中NO的物质的量是5mol,则v(NO)=$\frac{\frac{5mol}{5L}}{5min}$=0.2mol/(L.min);
N2(g)+O2(g)?2NO(g)
起始浓度(mol/L):1.3 1.5 0
变化浓度(mol/L):0.5 0.5 1
平衡浓度(mol/L):0.8 1 1
平衡常数K=$\frac{{c}^{2}(NO)}{c({N}_{2})×c({O}_{2})}$=$\frac{{1}^{2}}{0.8×1}$=1.25
故答案为:0.2mol/(L.min);1.25;
②a.混合气体总质量不变,容器容积不变,混合气体的密度始终不变,故a不符合;
b.随反应进行混合气体总物质的量不变,恒温恒容下,压强始终不变,故b不符合;
c.随反应进行反应物浓度减小,平衡前正反应速率减小,故c符合;
d.平衡之前,正反应速率大于逆反应速率,随反应进行,正反应速率减小,逆反应速率增大,故单位时间内,N2和NO的消耗量之比发生变化,故d符合,
故选:cd;
(2)已知:①N2(g)+O2(g)=2NO(g)△H=+180.5kJ•mol-1
②2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ•mol-1
根据盖斯定律,②-①可得:2H2(g)+2NO(g)=N2(g)+2H2O(l)△H=-752.1 kJ•mol-1,
故答案为:2H2(g)+2NO(g)=N2(g)+2H2O(l)△H=-752.1 kJ•mol-1;
(3)温度越高反应速率越快,到达平衡时间越短,故温度T2>T1,升高温度NO的浓度增大,说明平衡逆向移动,则正反应为放热反应,该反应的△H<0,
故答案为:<;
(4)A.电子由负极沿导线移向正极,Zn为负极,Cu为正极,故A正确;
B.取出盐桥后,处于断路状态,不能形成原电池,电流计不发生偏转,故B错误;
C.反应中,盐桥中K+会移向正极,即K+会移向CuSO4溶液,故C正确;
D.Cu为正极,发生还原反应,析出Cu,反应后铜片质量增加,故D正确.
故选:ACD.
点评 本题考查化学反应速率与化学平衡常数计算、化学平衡图象、热化学方程式书写、原电池原理等,侧重考查学生分析解决问题的能力、对知识的迁移运用能力.

 阅读快车系列答案
阅读快车系列答案
| A. | a是反应物 | B. | 正反应是一个体积扩大的反应 | ||
| C. | 若升高温度,a的转化率增大 | D. | 若增大压强,a的转化率减小 |
| A. | 在Na2CO3、NaHCO3两溶液中,离子种类不相同 | |
| B. | 在NaHCO3溶液中有c(H+)+c(Na+)=c(OH-)+c(CO32-)+c(HCO3-) | |
| C. | 在Na2CO3溶液中有c(OH-)=c(H+)+c(HCO3-)+2 c(H2CO3) | |
| D. | 在Na2CO3溶液中有2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
| A. | HCl和H2O | B. | O2和H2O | C. | NH3和H2O | D. | CO2和NaOH溶液 |
| A. | 浓硝酸和稀硝酸都具有氧化性 | B. | 铜与硝酸的反应属于置换反应 | ||
| C. | 硝酸可氧化Fe2+ | D. | 可用铁或铝制品盛装浓硝酸 |
| A. | 及时分离出NO2气体 | B. | 适当升高温度 | ||
| C. | 增大O2的浓度 | D. | 选择高效催化剂. |
| A. | 麦芽糖和蔗糖 | B. | 与 CH3-CH2-CH2-CH3 与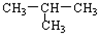 | ||
| C. | C2H6与C3H8 | D. | O2与O3 |
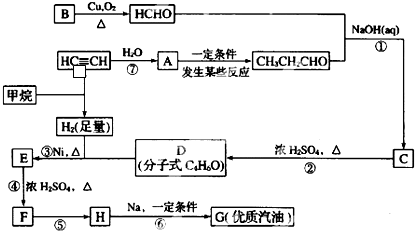
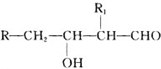
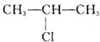
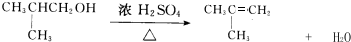 ;H→G
;H→G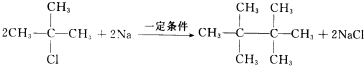 .
. .
.