题目内容
16.化学在日常生活中有着广泛的应用,下列对应项不存在因果关系的是( )| 物质性质 | 实际应用 | |
| A | 硅胶吸水能力强 | 食品、药品干燥剂 |
| B | 油脂在碱性条件下水解 | 制肥皂 |
| C | SiO2是酸性氧化物 | 光导纤维 |
| D | Na2O2与CO2、H2O反应 | 潜水艇中作为氧气来源 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.硅胶具有吸水性,而且无毒;
B.油脂在碱性条件下水解生成硬脂酸钠;
C.SiO2晶体对光具有全反射作用,能传递光信号;
D.Na2O2与CO2、H2O反应生成氧气.
解答 解:A.硅胶具有吸水性,而且无毒,能用作食品、药品干燥剂,故A正确;
B.油脂在碱性条件下水解生成硬脂酸钠,肥皂的主要成分是硬脂酸钠,则油脂在碱性条件下水解生成肥皂,故B正确;
C.SiO2晶体对光具有全反射作用,能传递光信号,能作光导纤维,故C错误;
D.Na2O2与CO2、H2O反应生成氧气,所以可以用作潜水艇中作为氧气来源,故D正确.
故选C.
点评 本题考查了化学在生产、生活中的应用,明确相关物质的性质是解题关键,题目难度不大,侧重于考查学生对基础知识的应用能力.

练习册系列答案
相关题目
4.T1 K时,向容积为2L的密闭容器中充入一定量的CO和H2O(g),发生反应:CO(g)+H2O(g)?CO2(g)+H2(g),反应过程中测定的部分数据如表(表中t2>t1)所示,下列说法错误的是( )
| 反应时间/min | n(CO)/mol | n(H2O)/mol |
| 0 | 2.00 | 3.00 |
| t1 | 0.80 | |
| t2 | 1.80 |
| A. | 用H2表示反应在t1 min内的平均速率为v(H2)=$\frac{0.60}{t_1}$mol•L-1•min-1 | |
| B. | 保持其他条件不变,t1时向容器中充入3.00 mol N2,达到平衡时,n(CO2)=1.20 mol | |
| C. | 保持其他条件不变,在t2 min时向容器中再通入1.00 mol CO,与原平衡相比,达到新平衡时CO的转化率将增大 | |
| D. | 温度升至T2 K,上述反应的平衡常数为0.70,则正反应的△H<0 |
1.下列元素非金属性最强的是( )
| A. | 硅 | B. | 磷 | C. | 硫 | D. | 砷 |
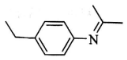
8.某有机物结构如图所示,有关该物质的叙述正确的是( )


| A. | 易溶于水 | |
| B. | 一氯代物有5种 | |
| C. | 最多能与氢气以物质的量之比1:4加成 | |
| D. | 碱性水解的产物之一是1-丙醇 |
5.下列各项应用涉及的化学原理完全相同的是( )
| A. | 用氯化铁或液氯处理废水 | |
| B. | 用铁槽车或铝槽车运输浓硫酸 | |
| C. | 用二氧化硫或氯气漂自织物 | |
| D. | 用亚硫酸钠或氯水处理二氧化硫尾气 |
6.设NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 7.1 g 37Cl2含有的中子数为4NA | |
| B. | NA个Al(OH)3胶体粒子的质量为78 g | |
| C. | 7.8 g Na2O2晶体中阴阳离子总数为0.3NA | |
| D. | 标准状况下,2.24 L己烷含有的共价键数为1.9NA |
 )有广泛应用.合成G的一种路径如图.1H-NMR谱显示C结构中只有一种环境的氢,且不能发生银镜反应,D的组成为C8H10.
)有广泛应用.合成G的一种路径如图.1H-NMR谱显示C结构中只有一种环境的氢,且不能发生银镜反应,D的组成为C8H10.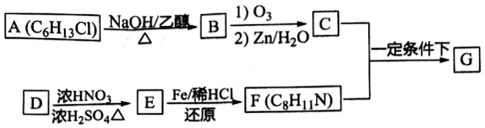
 $→_{②Zn/H_{2}O}^{①O_{3}}$R1CHO+
$→_{②Zn/H_{2}O}^{①O_{3}}$R1CHO+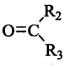
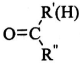 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$ +H2O
+H2O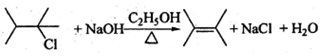 .
. .
.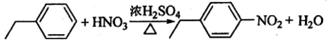 .
.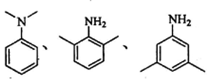 .
.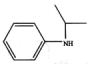 )的合成路线(流程图表示,无机试剂任选)
)的合成路线(流程图表示,无机试剂任选)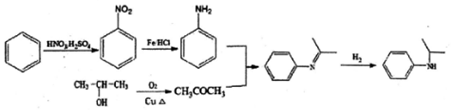 .
.