题目内容
11.某铁的氧化物1.52g溶于足量稀硫酸中,向所得溶液中通入标准状况下112mL SO3,恰好将Fe3+完全还原,则该氧化物的化学式为( )| A. | Fe2O3 | B. | Fe3O4 | C. | Fe4O5 | D. | Fe6O7 |
分析 设铁的氧化物为FexOy,根据电子守恒可知,FexOy被还原Fe3+转移的电子数和SO3转移的电子数相等.
解答 解:FexOy中Fe的平均化合价为+$\frac{2y}{x}$,被还原为Fe2+,根据电子守恒可知,转移的电子数和SO3转移的电子数相等.标准状况下112mL SO3转移电子数为$\frac{0.112L}{22.4L/mol}$×2=0.01mol.则有:$\frac{1.52g}{(56x+16y)g/mol}$×($\frac{2y}{x}$-2)×x=0.01mol,解得$\frac{x}{y}$=$\frac{4}{5}$,
故选:C.
点评 本题考查氧化还原反应计算,注意氧化还原反应计算中电子转移守恒运用,本题中注意平均化合价的应用,侧重考查学生的分析计算能力.

练习册系列答案
相关题目
1.水煤气法制甲醇工艺流程框图如图:
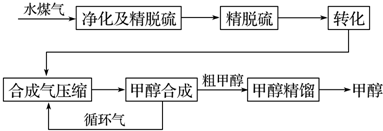
已知:除去水蒸气后的水煤气含55~59%的H2,15~18%的CO,11~13%的CO2,少量的H2S、CH4,除去H2S后,可采用催化或非催化转化技术,将CH4转化成CO,得到CO、CO2和H2的混合气体,是理想的合成甲醇原料气,即可进行甲醇合成.
(1)制水煤气的主要化学反应方程式为C(s)+H2O(g)?CO(g)+H2(g),此反应是吸热反应.
①此反应的化学平衡常数表达式为$\frac{[CO]•[{H}_{2}]}{[{H}_{2}O]}$;
②下列能提高碳的平衡转化率的措施是BC.
A加入C(s) B.加入H2O(g) C.升高温度 D.增大压强
(2)将CH4转化成CO,工业上常采用催化转化技术,其反应原理为CH4(g)+$\frac{3}{2}$O2(g)?CO(g)+2H2O(g)△H=-519kJ.工业上要选择合适的催化剂,分别对X、Y、Z三种催化剂进行如下实验(其他条件相同).
①X在T1℃时催化效率最高,能使正反应速率加快约3×105倍;
②Y在T2℃时催化效率最高,能使正反应速率加快约3×105倍;
③Z在T3℃时催化效率最高,能使逆反应速率加快约1×106倍;
已知:T1>T2>T3,根据上述信息,你认为在生产中应该选择的适宜催化剂是Z(填“X”或“Y”或“Z”),选择的理由是催化活性高、速度快、反应温度较低.
(3)合成气经压缩升温后进入10m3甲醇合成塔,在催化剂作用下,进行甲醇合成,主要反应是:2H2(g)+CO(g)?CH3OH(g)△H=-181.6kJ.4℃下此反应的平衡常数为160.此温度下,在密闭容器中加入CO、H2,反应到某时刻测得各组分的浓度如下:
①比较此时正、逆反应速率的大小:v正>v逆(填“>”、“<”或“=”).
②若加入同样多的CO、H2,在T5℃反应,10min后达到平衡,此时c(H2)=0.4mol•L-1,则该时间内反应速率v(CH3OH)=0.03mol•L-1•min-1.
(4)生产过程中,合成气要进行循环,其目的是提高原料利用率(或提高产量、产率亦可).

已知:除去水蒸气后的水煤气含55~59%的H2,15~18%的CO,11~13%的CO2,少量的H2S、CH4,除去H2S后,可采用催化或非催化转化技术,将CH4转化成CO,得到CO、CO2和H2的混合气体,是理想的合成甲醇原料气,即可进行甲醇合成.
(1)制水煤气的主要化学反应方程式为C(s)+H2O(g)?CO(g)+H2(g),此反应是吸热反应.
①此反应的化学平衡常数表达式为$\frac{[CO]•[{H}_{2}]}{[{H}_{2}O]}$;
②下列能提高碳的平衡转化率的措施是BC.
A加入C(s) B.加入H2O(g) C.升高温度 D.增大压强
(2)将CH4转化成CO,工业上常采用催化转化技术,其反应原理为CH4(g)+$\frac{3}{2}$O2(g)?CO(g)+2H2O(g)△H=-519kJ.工业上要选择合适的催化剂,分别对X、Y、Z三种催化剂进行如下实验(其他条件相同).
①X在T1℃时催化效率最高,能使正反应速率加快约3×105倍;
②Y在T2℃时催化效率最高,能使正反应速率加快约3×105倍;
③Z在T3℃时催化效率最高,能使逆反应速率加快约1×106倍;
已知:T1>T2>T3,根据上述信息,你认为在生产中应该选择的适宜催化剂是Z(填“X”或“Y”或“Z”),选择的理由是催化活性高、速度快、反应温度较低.
(3)合成气经压缩升温后进入10m3甲醇合成塔,在催化剂作用下,进行甲醇合成,主要反应是:2H2(g)+CO(g)?CH3OH(g)△H=-181.6kJ.4℃下此反应的平衡常数为160.此温度下,在密闭容器中加入CO、H2,反应到某时刻测得各组分的浓度如下:
| 物质 | H2 | CO | CH3OH |
| 浓度/mol•L-1 | 0.2 | 0.1 | 0.4 |
②若加入同样多的CO、H2,在T5℃反应,10min后达到平衡,此时c(H2)=0.4mol•L-1,则该时间内反应速率v(CH3OH)=0.03mol•L-1•min-1.
(4)生产过程中,合成气要进行循环,其目的是提高原料利用率(或提高产量、产率亦可).
6.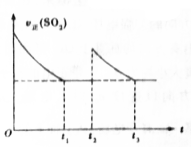 一定温度下,密闭容器中进行反应:2SO2(g)+O2(g)?2SO3(g)△H<0.测得v正(SO2)随反应时间(t)的变化如图所示.下列有关说法正确的是( )
一定温度下,密闭容器中进行反应:2SO2(g)+O2(g)?2SO3(g)△H<0.测得v正(SO2)随反应时间(t)的变化如图所示.下列有关说法正确的是( )
 一定温度下,密闭容器中进行反应:2SO2(g)+O2(g)?2SO3(g)△H<0.测得v正(SO2)随反应时间(t)的变化如图所示.下列有关说法正确的是( )
一定温度下,密闭容器中进行反应:2SO2(g)+O2(g)?2SO3(g)△H<0.测得v正(SO2)随反应时间(t)的变化如图所示.下列有关说法正确的是( )| A. | t2时改变的条件是:只加入一定量的SO2 | |
| B. | t1时平衡常数K1大于t3时平衡常数K2 | |
| C. | t1时平衡混合气的$\overline{{M}_{1}}$大于t3时平衡混合气的$\overline{{M}_{2}}$ | |
| D. | t1时平衡混合气中的SO3的体积分数等于t3时平衡混合气中SO3的体积分数 |
16.设NA为阿伏加德罗常数值,下列说法正确的是( )
| A. | 1 L 0.5 mol/L NaHCO3溶液中含有的HCO3-数目小于0.5 NA | |
| B. | 11.2 g 铁粉与硝酸反应失去电子数一定为0.6 NA | |
| C. | 25℃时,pH=13的 Ba(OH)2溶液中含有的OH-数目为0.2 NA | |
| D. | 46 g甲苯含有C=C双键的数目为1.5 NA |
2.下列实验能获得成功的是( )
| A. | 无水乙酸和乙醇共热制取乙酸乙酯 | |
| B. | 将苯逐滴滴入浓硝酸中,并用沸水浴加热制取硝基苯 | |
| C. | 将铜丝在酒精灯上加热后,立即伸人无水乙醇中,铜丝恢复原来的红色 | |
| D. | 淀粉用酸催化水解后的溶液加入新制银氨溶液,水浴加热,可看到有银镜出现 |
3.工业废气H2S经资源利用后可回收能量并得到单质硫.反应原理如图所示.下列说法不正确的是( )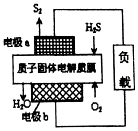

| A. | 电极a为电池的负极 | |
| B. | 电极b上发生的电极反应为O2+4H++4e-═2H2O | |
| C. | 若电路中通过2mol电子,则电池内部释放632kJ热量 | |
| D. | 若有17gH2S参与反应,则会有1molH+经质子膜进入正极区 |

