题目内容
下列各组物质中,都是共价化合物的是( )
| A、H2S和Na2O2 |
| B、H2O2和CaF2 |
| C、CO2和N2 |
| D、HNO3和HClO3 |
考点:共价键的形成及共价键的主要类型
专题:
分析:只含有共价键的化合物叫做共价化合物,含有离子键的化合物叫做离子化合物,以此分析.
解答:
解:A、过氧化钠是由钠离子和过氧根离子以离子键结合形成的离子化合物,故A不选;
B、氟化钙是由钙离子和氟离子以离子键结合形成的离子化合物,故B不选;
C、氮气属于单质,不是化合物,故C不选;
D、HNO3和HClO3都是以共用电子对结合形成的化合物,只含有共价键,属于共价化合物,故D选.
故选D.
B、氟化钙是由钙离子和氟离子以离子键结合形成的离子化合物,故B不选;
C、氮气属于单质,不是化合物,故C不选;
D、HNO3和HClO3都是以共用电子对结合形成的化合物,只含有共价键,属于共价化合物,故D选.
故选D.
点评:本题考查了共价化合物和离子化合物的判断,题目难度不大,注意由共价键组成的化合物叫做共价化合物,含有离子键的化合物叫做离子化合物.

练习册系列答案
相关题目
下列说法正确的是( )
| A、摩尔是物质的质量单位 |
| B、氢气的摩尔质量是2 g |
| C、1mo1 0H-的质量是17 g |
| D、1mol气体所占的体积一定是22.4L |
下列物质中,含有离子键的化合物是( )
| A、H2 |
| B、N2 |
| C、NaCl |
| D、Fe |
下列排序正确的是( )
| A、酸性:H2CO3>CH3COOH |
| B、碱性:Ba(OH)2<Ca(OH)2<KOH |
| C、熔点:MgBr2<SiCl4 |
| D、沸点:PH3<NH3<H2O |
下列分子中的碳原子一定处于同一平面的是( )
A、 |
B、 |
| C、CH≡CCH2CH3 |
| D、CH3CH=CHCHO |
镭是元素周期表中第七周期ⅡA族元素,下列关于镭的叙述不正确的是( )
| A、镭比钙的金属性更强 |
| B、在化合物中呈+2价 |
| C、镭是一种放射性元素 |
| D、氢氧化镭呈两性 |
14.5g某烷烃完全燃烧生成1.25mol H2O,则该烃的一氯代物共有(不考虑立体异构)( )
| A、2种 | B、3种 | C、4种 | D、5种 |
下列水解化学方程式或水解离子方程式正确的是( )
| A、CH3COO-+H2O?CH3COOH+OH- |
| B、NH4++H2O?NH4OH+H+ |
| C、CH3COOH+H2O?CH3COO-+H3O+ |
| D、NaCl+H2O?NaOH+HCl |
如图是产生和收集气体的装置,该装置最适合于( )
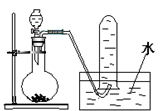

| A、用浓硝酸与铜反应制取NO2 |
| B、用H2O2溶液和MnO2反应制取O2 |
| C、用浓盐酸和MnO2反应制取Cl2 |
| D、用氯化铵和氢氧化钙反应制取NH3 |