题目内容
“封管实验”具有简易、方便、节约、绿色等优点.观察下列四个“封管实验”(夹持装置未画出),判断下列说法正确的是( )


| A、加热时,a上部聚集了固体NH4Cl,说明NH4Cl的热稳定性比较好 |
| B、加热时,发现b中I2变为紫色蒸气,在上部又聚集为紫黑色固体 |
| C、加热时,c中溶液红色变深,冷却后又逐渐变浅 |
| D、水浴时,d内气体颜色加深,e内气体颜色变浅 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.氯化铵分解生成氨气和氯化氢,氯化氢和氨气反应又生成氯化铵;
B.加热碘升华,在上部冷却到达碘的固体;
C.温度升高气体的溶解度降低,根据氨气使酚酞变红的原理解答;
D.根据温度对平衡移动影响分析二氧化氮的浓度变化,据此解答.
B.加热碘升华,在上部冷却到达碘的固体;
C.温度升高气体的溶解度降低,根据氨气使酚酞变红的原理解答;
D.根据温度对平衡移动影响分析二氧化氮的浓度变化,据此解答.
解答:
解:A.加热时氯化铵分解生成氨气和氯化氢,在试管的顶部氨气和氯化氢又反应生成氯化铵,NH4Cl的热稳定性较差,故A错误;
B.加热碘升华,变为紫色蒸气,在上部冷却聚集为紫黑色的碘固体,故B正确;
C.氨水显碱性,使酚酞变红,加热时,氨气逸出,溶液红色变浅,冷却后,氨气又溶于水和水反应,溶液红色又变深,故C错误;
D.存在平衡2NO2 (g)?N2O4(g)△H=-92.4kJ/mol,正反应为放热反应,d浸泡在热水中,升高温度平衡向逆反应方向移动,二氧化氮浓度减小,d容器内气体颜色变深,e浸泡在冷水中,二氧化氮浓度增大,温度降低平衡向正反应移动,e容器内气体颜色变浅,故D正确;
故选BD.
B.加热碘升华,变为紫色蒸气,在上部冷却聚集为紫黑色的碘固体,故B正确;
C.氨水显碱性,使酚酞变红,加热时,氨气逸出,溶液红色变浅,冷却后,氨气又溶于水和水反应,溶液红色又变深,故C错误;
D.存在平衡2NO2 (g)?N2O4(g)△H=-92.4kJ/mol,正反应为放热反应,d浸泡在热水中,升高温度平衡向逆反应方向移动,二氧化氮浓度减小,d容器内气体颜色变深,e浸泡在冷水中,二氧化氮浓度增大,温度降低平衡向正反应移动,e容器内气体颜色变浅,故D正确;
故选BD.
点评:本题以“封管实验”为载体,考查元素化合物性质、化学平衡影响因素等,难度中等,注意基础知识的理解掌握.

练习册系列答案
相关题目
 向MgCl2和AlCl3的混合溶液中加入氢氧化钠溶液,所得沉淀的物质的量(n)与加入氢氧化钠溶液的体积(V)关系如图所示.则下列说法正确的是( )
向MgCl2和AlCl3的混合溶液中加入氢氧化钠溶液,所得沉淀的物质的量(n)与加入氢氧化钠溶液的体积(V)关系如图所示.则下列说法正确的是( )| A、b、c两点沉淀物成分相同,d、e两点沉淀物成分相同 |
| B、在反应过程中,各状态点溶液的pH大小顺序是:e>d>c>a>b |
| C、b-c段与c-d段溶液中阴离子的物质的量相等 |
| D、在d点,向溶液中逐滴加入盐酸,沉淀量将减少 |
已知NH3极易溶于水,下列组合中不能形成喷泉的是( )
| A、HCl和H2O |
| B、O2和H2O |
| C、NH3和H2O |
| D、CO2和NaOH |
金刚石、石墨物理性质不同的原因是( )
| A、组成的元素不同 |
| B、金刚石是单质,石墨是化合物 |
| C、碳原子结构不同 |
| D、碳原子的排列方式不同 |
物质的量浓度相同的下列溶液,pH由大到小排列正确的是( )
| A、Ba(OH)2、Na2SO3、FeCl3、KCl |
| B、Na2CO3、NaHCO3、KNO3、NH4Cl |
| C、NH3?H2O、H3PO4、Na2SO4、H2SO4 |
| D、HCl、CH3COOH、C2H5OH、Na2SiO3 |
实验操作的规范是实验的基本要求,下列实验操作正确的是( )
A、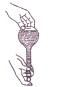 检验容量瓶是否漏水 |
B、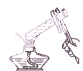 给溶液加热 |
C、 滴加液体 |
D、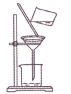 过滤 |
下列说法正确的是( )
| A、丙烷是直链烃,所以分子中3个碳原子也在一条直线上 |
| B、丙烯所有原子均在同一平面上 |
C、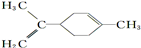 所有碳原子一定在同一平面上 所有碳原子一定在同一平面上 |
D、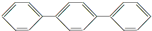 至少有16个原子共平面 至少有16个原子共平面 |
氯化溴(BrCl)和Br2、Cl2具有相似的性质,下列有关氯化溴性质的判断中错误的是( )
| A、在CCl4中的溶解性BrCl<Br2 |
| B、BrCl氧化性比Br2强,比Cl2弱 |
| C、沸点BrCl>Br2 |
| D、常温下BrCl可与NaOH溶液反应生成NaCl和NaBrO |