题目内容
如下图所示,用石墨作电极进行电解,电解槽甲中盛AgNO3溶液,电解槽乙中盛有含二价金属G的氯化物溶液1 L,其物质的量浓度为0.1 mol/L,当通电一段时间后,电解槽甲中阴极增重0.27 g,乙中阴极增重0.14 g,则元素G的相对原子质量为( )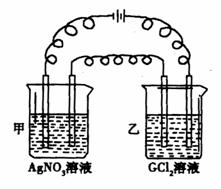
A.112 B.73 C.64 D.65
A
【解析】 本题考查守恒规律的应用;阴极增重是因为甲中析出了银,乙中析出了G。根据串联电路中通过的电子相等:0.27×1/108=0.14×2/R(G)求出G的相对原子质量R(G)=112。

练习册系列答案
相关题目
 碳和碳的化合物在生产、生活中的应用非常广泛,在提倡健康生活已成潮流的今天,“低碳生活”不再只是一种理想,更是一种值得期待的新的生活方式.
碳和碳的化合物在生产、生活中的应用非常广泛,在提倡健康生活已成潮流的今天,“低碳生活”不再只是一种理想,更是一种值得期待的新的生活方式.