题目内容
20.己知:60℃时,KNO3的溶解度为110g.在此温度下,向盛有l00mL水的烧杯中投入101g KNO3后充分搅拌,此烧杯中将会得到( )| A. | 悬浊液 | B. | 饱和溶液 | ||
| C. | 质量分数约为50%的溶液 | D. | 物质的量浓度为10mol/L的溶液 |
分析 溶解度为饱和时100g水中溶解溶质的质量,向盛有l00mL水的烧杯中投入101g KNO3后充分搅拌,没有达到饱和,此时n(KNO3)=$\frac{101g}{101g/mol}$=1mol,结合溶液的体积解答该题.
解答 解:A.60℃时,KNO3的溶解度为110g,101<110,不是悬浊液,故A错误;
B.101<110,则溶液没有达到饱和,故B错误;
C.质量分数为$\frac{101}{100+101}×100%$≈50%,故C正确;
D.n(KNO3)=$\frac{101g}{101g/mol}$=1mol,而溶液体积大于100mL,则质的量浓度小于10mol/L的溶液,故D错误.
故选C.
点评 本题考查物质的浓度的计算,为高频考点,侧重考查学生的分析能力和计算能力,注意理解溶解度的概念,易错点为D,注意溶液的体积,难度不大.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目
18.用含钴废料(含CoCO3、少量NiCO3与铁屑)制备CoCl2•6H2O的工艺流程如图1:
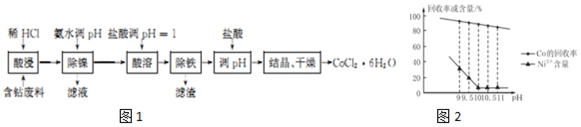
已知:除镍过程中溶液pH对Co的冋收率影响如图2所示;部分金属离子在实验条件下开始沉淀和完全沉淀的pH如表所示.
(1)酸浸工艺中用“稀HCl”替代了传统的“盐酸与硝酸的混酸”,其优点为减少有毒气体氮氧化物的排放;防止产品中混有硝酸盐(或防止将Co2+氧化).
(2)除镍时应调节pH=10;此步骤中Ni2+是否形成Ni(OH)2沉淀?否.
(3)除铁过程包括以下多个步骤:①向溶液中滴加适量30%H2O2,使其充分反应;②向溶液中加入CoCO3,调节溶液pH4.l≤pH<6.6,使Fe3+沉淀完全;③过滤得CoCl2溶液. (可供选用的试剂:30% H2O2、l.0mol•L-1KMnO4、NaOH固体、CoCO3固体)
(4)除铁后加入盐酸调pH的作用是抑制Co2+水解.
(5)工业上采用减压蒸干的方法制备CoCl2•6H2O,减压蒸干的目的是防止CoCl2•6H2O分解.

已知:除镍过程中溶液pH对Co的冋收率影响如图2所示;部分金属离子在实验条件下开始沉淀和完全沉淀的pH如表所示.
| 金属离子 | 开始沉淀的pH | 完全沉淀的pH |
| Fe3+ | 1.5 | 4.1 |
| Fe2+ | 7.5 | 9.7 |
| Co2+ | 6.6 | 9.4 |
| Ni2+ | 6.7 | 9.5 |
(2)除镍时应调节pH=10;此步骤中Ni2+是否形成Ni(OH)2沉淀?否.
(3)除铁过程包括以下多个步骤:①向溶液中滴加适量30%H2O2,使其充分反应;②向溶液中加入CoCO3,调节溶液pH4.l≤pH<6.6,使Fe3+沉淀完全;③过滤得CoCl2溶液. (可供选用的试剂:30% H2O2、l.0mol•L-1KMnO4、NaOH固体、CoCO3固体)
(4)除铁后加入盐酸调pH的作用是抑制Co2+水解.
(5)工业上采用减压蒸干的方法制备CoCl2•6H2O,减压蒸干的目的是防止CoCl2•6H2O分解.
8.下列说法正确的是( )
| A. | 浓硫酸在常温下可迅速与铜片反应放出二氧化硫气体 | |
| B. | 在含有Cu(NO3)2、Mg(NO3)2和AgNO3的溶液中加入适量锌粉,首先置换出的是Cu | |
| C. | 能与酸反应生成盐和水的氧化物一定是碱性氧化物 | |
| D. | 将Ba(OH)2溶液滴到明矾溶液中,当SO42-刚沉淀完时,铝以AlO2-的形式存在 |
9.下面有关pH的说法正确的是( )
| A. | 在pH=12的溶液中.水电离出的c(OH-)定等于10-12mol/L | |
| B. | 将pH=2和pH=l2的酸碱溶液等体积混合后,溶液的pH一定等于7 | |
| C. | 若强酸、强碱中和后pH=7,则中和之前酸、碱的pH之和一定等于14 | |
| D. | 含等物质的量的HNO3、Na2CO3、CH3COOH的溶液混合后.溶液的pH一定大于7 |
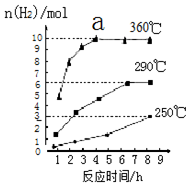 磷化氢气体(PH3)是一种强烈的储粮杀虫剂,其制取原理类似于实验室制氨气,空气中磷化氢气体达到2PPM以上是就会造成人畜中毒,请回答:
磷化氢气体(PH3)是一种强烈的储粮杀虫剂,其制取原理类似于实验室制氨气,空气中磷化氢气体达到2PPM以上是就会造成人畜中毒,请回答: .
.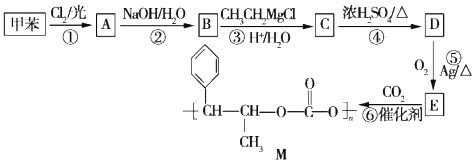
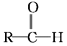 +R′-MgX→
+R′-MgX→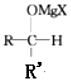 $\stackrel{H+/H_{2}O}{→}$
$\stackrel{H+/H_{2}O}{→}$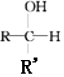 (R,R'均为烃基);
(R,R'均为烃基);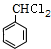 ,D
,D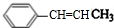 ,E
,E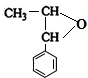 .
. .B与新制的Cu(OH)2悬浊液共热反应
.B与新制的Cu(OH)2悬浊液共热反应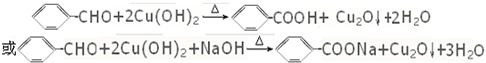 .
.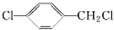 (填结构简式).
(填结构简式).