题目内容
为了测定某有机物A的结构,做如下实验:
①将2.3g该有机物完全燃烧,生成0.1mol CO2和2.7g水;
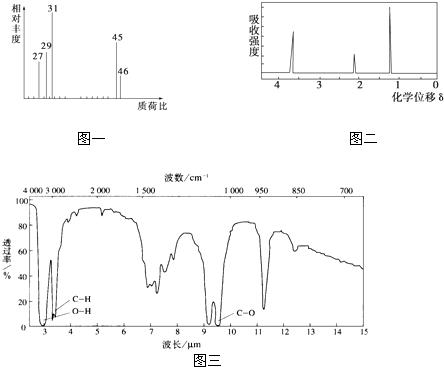
②用质谱仪测定其相对分子质量,得如图一所示的质谱图;
③用核磁共振仪处理该化合物,得到如图二所示图谱,图中三个峰的面积之比是1:2:3.
④用红外光谱仪处理该化合物,得到如图三所示图谱.
试回答下列问题:
(1)有机物A的相对分子质量是 .
(2)有机物A的实验式是 .
(3)有机物A的分子式是 .
(4)有机物A的结构简式是 .
①将2.3g该有机物完全燃烧,生成0.1mol CO2和2.7g水;
②用质谱仪测定其相对分子质量,得如图一所示的质谱图;
③用核磁共振仪处理该化合物,得到如图二所示图谱,图中三个峰的面积之比是1:2:3.
④用红外光谱仪处理该化合物,得到如图三所示图谱.
试回答下列问题:

(1)有机物A的相对分子质量是
(2)有机物A的实验式是
(3)有机物A的分子式是
(4)有机物A的结构简式是
考点:有机物实验式和分子式的确定,常见有机化合物的结构
专题:有机化学基础
分析:(1)根据质合比可知,该有机物A的相对分子量为46;
(2)根据2.3g该有机物充分燃烧生成的二氧化碳、水的量判断有机物A中的碳元素、氢元素的物质的量、质量,再判断是否含有氧元素,计算出C、H、O元素的物质的量之比,最后确定A的分子式;
(3)因为实验式是C2H6O的有机物中,氢原子数已经达到饱和,所以其实验式即为分子式;
(4)结合核磁共振氢谱判断该有机物分子的结构简式.
(2)根据2.3g该有机物充分燃烧生成的二氧化碳、水的量判断有机物A中的碳元素、氢元素的物质的量、质量,再判断是否含有氧元素,计算出C、H、O元素的物质的量之比,最后确定A的分子式;
(3)因为实验式是C2H6O的有机物中,氢原子数已经达到饱和,所以其实验式即为分子式;
(4)结合核磁共振氢谱判断该有机物分子的结构简式.
解答:
解:(1)在A的质谱图中,最大质荷比为46,所以其相对分子质量也是46,
故答案为:46;
(2)2.3 g该有机物中,n(C)=n(CO2)=0.1 mol,含有的碳原子的质量为m(C)=0.1 mol×12 g?mol-1=1.2 g,
氢原子的物质的量为:n(H)=
×2=0.3 mol,氢原子的质量为m(H)=0.3 mol×1 g?mol-1=0.3 g,
该有机物中m(O)=2.3 g-1.2 g-0.3 g=0.8 g,氧元素的物质的量为n(O)=
=0.05 mol,
则n(C):n(H):n(O)=0.1 mol:0.3 mol:0.05 mol=2:6:1,所以A的实验式是:C2H6O,
故答案为:C2H6O;
(3)因为实验式是C2H6O的有机物中,氢原子数已经达到饱和,所以其实验式即为分子式,
故答案为:C2H6O;
(4)A有如下两种可能的结构:CH3OCH3或CH3CH2OH;若为前者,则在核磁共振氢谱中应只有1个峰;若为后者,则在核磁共振氢谱中应有3个峰,而且3个峰的面积之比是1:2:3,显然CH3CH2OH符合题意,所以A为乙醇,
故答案为:CH3CH2OH.
故答案为:46;
(2)2.3 g该有机物中,n(C)=n(CO2)=0.1 mol,含有的碳原子的质量为m(C)=0.1 mol×12 g?mol-1=1.2 g,
氢原子的物质的量为:n(H)=
| 2.7g |
| 18g/mol |
该有机物中m(O)=2.3 g-1.2 g-0.3 g=0.8 g,氧元素的物质的量为n(O)=
| 0.8g |
| 16g/mol |
则n(C):n(H):n(O)=0.1 mol:0.3 mol:0.05 mol=2:6:1,所以A的实验式是:C2H6O,
故答案为:C2H6O;
(3)因为实验式是C2H6O的有机物中,氢原子数已经达到饱和,所以其实验式即为分子式,
故答案为:C2H6O;
(4)A有如下两种可能的结构:CH3OCH3或CH3CH2OH;若为前者,则在核磁共振氢谱中应只有1个峰;若为后者,则在核磁共振氢谱中应有3个峰,而且3个峰的面积之比是1:2:3,显然CH3CH2OH符合题意,所以A为乙醇,
故答案为:CH3CH2OH.
点评:本题考查了有机物分子式、结构简式的计算方法,题目难度中等,注意根据质量守恒确定有机物分子式的方法,明确质量比、核磁共振氢谱的含义是解题关键.

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案
相关题目
用NA表示阿伏加德罗常数,下列叙述正确的是( )
| A、64 g SO2含有氧原子数为1NA |
| B、物质的量浓度为0.5 mol?L-1的MgCl2溶液,含有Cl-数目为1 NA |
| C、标准状况下,22.4 L H2O的分子数为1N |
| D、常温常压下,14 g N2含有分子数为0.5 NA |
某气态烃0.5mol能与0.5molHCl完全加成,加成后的产物分子上的氢原子又可被2.5molCl2完全取代.则此气态烃可能是( )
| A、HC≡CH |
| B、CH2=CH2 |
| C、HC≡C-CH3 |
| D、CH2=C(CH3)CH3 |
 室温下,用0.100mol/L 盐酸溶液滴定20.00mL 0.100mol/L的某氨水溶液,滴定曲线如图所示,下列有关说法不正确的是( )
室温下,用0.100mol/L 盐酸溶液滴定20.00mL 0.100mol/L的某氨水溶液,滴定曲线如图所示,下列有关说法不正确的是( )| A、曲线上除d点外任意一点所示溶液中:c(NH4+)+c(H+)=c(Cl- )+c(OH - ) |
| B、a点所示溶液中,c(Cl-)>c(NH4+ )>c(NH3?H2O)>c(OH- )>c(H+ ) |
| C、b点所示溶液中,c(NH4+)=c(Cl-) |
| D、c点所示溶液中,c(Cl- )>c(NH4+)>c(H+)>c(NH3?H2O) |
 1mol C6H6与H2加成时:Ⅰ需
1mol C6H6与H2加成时:Ⅰ需 立体结构:该结构的二氯代物有
立体结构:该结构的二氯代物有 )脱去2mol氢原子变成苯却放热,可推断苯比1,3-环己二烯
)脱去2mol氢原子变成苯却放热,可推断苯比1,3-环己二烯