题目内容
4.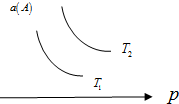 在一定条件下,某可逆反应aA(g)+bB(s)?cC(g)达到平衡后,A的转化率a(A)与温度(T)、压强(p)的关系如图所示,根据图象,下列判断正确的是( )
在一定条件下,某可逆反应aA(g)+bB(s)?cC(g)达到平衡后,A的转化率a(A)与温度(T)、压强(p)的关系如图所示,根据图象,下列判断正确的是( )| A. | a+b<c | |
| B. | 若T2>T1,则该反应在高温下易自发进行 | |
| C. | △H>0 | |
| D. | 若T2<T1,则该反应一定不能自发进行 |
分析 由图象曲线变化可知,温度一定,随着压强的增大,A的转化率a(A)降低,说明增大压强平衡向逆反应方向移动,说明逆反应是气体体积缩小的反应,说明a<c,根据据△H-T△S<0,来判断反应的自发性,以此解答该题.
解答 解:A、温度一定,随着压强的增大,A的转化率a(A)降低,说明增大压强平衡向逆反应方向移动,说明逆反应是气体体积缩小的反应,说明a<c,故A错误;
B、若T2>T1,则温度越高,A的转化率a(A)越大,说明平衡正向移动,正反应是吸热反应,所以△H>0,而△S>0,据据△H-T△S<0,该反应在高温下易自发进行,故B正确;
C、T2和T1的相对大小不知,所以无法求反应的热效应,故C错误;
D、若T2<T1,则温度越高,A的转化率a(A)越小,说明平衡逆向移动,正反应是放热反应,所以△H<0,而△S>0,所以△H-T△S<0,则该反应一定能自发进行,故D错误;
故选B.
点评 本题涉及图象的分析及化学平衡的移动和反应进行的方向等知识点,整合性较强,据据△H-T△S<0,来判断反应的自发性,题目难度中等.

练习册系列答案
相关题目
6.下列有关物质的性质或用途的叙述中,正确的是( )
| A. | 常温下,运输浓硫酸、浓硝酸时可用铝制或铁制槽车 | |
| B. | 用氯化钡溶液可区别SO42-和CO32-离子 | |
| C. | CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 | |
| D. | 二氧化硅是一种酸性氧化物,它不跟任何酸发生反应 |
4.已知3X(g)+2Y(g)?nZ(g)+2W(g),若将0.6mol X和0.4mol Y混合充入一密闭体积可调的容器中,压强保持不变,5min后体积变为原来的1.2倍,则n值是( )
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
11.已知氯仿通常是无色液体,不溶于水,密度约为水的1.5倍,沸点为61.2℃.要从水与氯仿的混合物中分离出氯仿,最合适的方法是( )
| A. | 蒸馏 | B. | 分液 | C. | 重结晶 | D. | 过滤 |
9.下列实验设计和结论相符的是( )
| A. | 将碘水倒入分液漏斗,加适量乙醇,振荡后静置,可将碘萃取到乙醇中 | |
| B. | 某气体能使湿润的红色石蕊试纸变蓝,该气体的水溶液一定呈碱性 | |
| C. | 某无色溶液中加入BaCl2溶液,再加稀盐酸,沉淀不溶解,原溶液中一定有SO42- | |
| D. | 某无色溶液中加入酚酞试液变红,该溶液一定是碱溶液 |
16.下列说法正确的是( )
| A. | 溶液和胶体的本质区别是丁达尔效应 | |
| B. | 液氨、氨水属于纯净物,盐酸和豆浆属于混合物 | |
| C. | 胶体区别于其它分散系的本质特征是粒子大小 | |
| D. | 能进行“交叉分类”的就不能进行“树状分类” |
14.阿伏加德罗曾做过这样一个实验:“一抽真空的密闭容器重M g,在标准状况下,盛满以相同物质的量混合的NO和H2的混合气体后,称量为(M+Q)g.把混合气体排尽,再充满SO2气体,为使天平平衡,应在托盘天平的_边托盘上放置_ g砝码…”横线上分别应填的是( )
| A. | 右 (M+2Q) | B. | 左 (M+2Q) | C. | 右 (M+4Q) | D. | 左 (M+4Q) |
 .
.