题目内容
17.下列离子方程式正确的是( )| A. | 用铜电极电解饱和食盐水:2Cl-+2H2O$\frac{\underline{\;点燃\;}}{\;}$H2↑+Cl2↑+2OH- | |
| B. | 向Na2SiO3溶液中加入盐酸:Na2SiO3+2H+═H2SiO3(胶体)+2Na+ | |
| C. | 向 溶液中通入少量CO2:2 溶液中通入少量CO2:2 +H2O+CO2→2 +H2O+CO2→2 +CO32- +CO32- | |
| D. | 向Mg(OH)2悬浊液中加入饱和NH4Cl溶液:2NH4++Mg(OH)2═2NH•H2O+Mg2+ |
分析 A.铜为电极,阳极铜失去电子生成铜离子,阴极氢离子得到电子生成氢气,反应生成氢气和氢氧化铜;
B.硅酸钠为易溶的强电解质,离子方程式中需要拆开;
C.碳酸氢根离子的酸性小于苯酚,苯酚钠与二氧化碳反应生成碳酸氢钠和苯酚,且苯酚钠小于拆开;
D.氢氧化镁为中强碱,则氢氧化钠能够与氯化铵溶液反应生成一水合氨和氯化镁.
解答 解:A.用铜电极电解饱和食盐水,阳极铁放电,阴极水电离出的氢离子放电生成氢气,则正确的离子方程式为:Cu+2H2O$\frac{\underline{\;电解\;}}{\;}$Cu(OH)2↓+H2↑,故A错误;
B.向Na2SiO3溶液中加入盐酸,反应生成硅酸胶体和氯化钠,硅酸钠应该拆开,正确的离子方程式为:SiO32-+2H+═H2SiO3(胶体),故B错误;
C.苯酚的酸性大于碳酸氢根离子,所以苯酚钠通入二氧化碳生成苯酚和碳酸氢钠,反应的离子方程式为:C6H5O-+CO2+H2O→C6H6OH+HCO3-,故C错误;
D.氢氧化镁的碱性大于一水合氨,二者反应生成一水合氨和氯化镁,反应的离子方程式为:2NH4++Mg(OH)2═2NH•H2O+Mg2+,故D正确;
故选D.
点评 本题考查了离子方程式的书写,题目难度中等,明确离子方程式的书写原则为解答关键,C为易错点,注意苯酚的酸性大于碳酸氢根离子,无论二氧化碳是否过量,反应都生成碳酸氢钠和苯酚.

练习册系列答案
相关题目
8.下列物质间反应的离子方程式正确的是( )
| A. | 相同物质的量浓度的FeI2溶液与溴水等体积混合 2Fe2++2I-+2Br2═2Fe3++I2+4Br- | |
| B. | Ba(OH)2溶液中加入过量的NaHSO4溶液 Ba2++OH-+H++SO42-═H2O+BaSO4↓ | |
| C. | 氢氧化亚铁溶液于稀硝酸中 Fe(OH)2+2H+═Fe2++2H2O | |
| D. | 向漂白粉溶液中通入少量的二氧化碳 Ca2++2ClO-+CO2+H2O═CaCO3↓+2HClO |
12.氨水的物质的量比为0.25,而它的摩尔分数应为( )
| A. | 0.15 | B. | 0.20 | C. | 0.25 | D. | 0.30 |
2.将10g铁碳合金放入O2中高温灼烧,反应后的气体通入到过量石灰水中得沉淀1.4g.则此铁碳合金是( )
| A. | 生铁 | B. | 高碳钢 | C. | 中碳钢 | D. | 低碳钢 |
4.下列说法中正确的是( )
| A. | 氯化钾溶液在电流作用下电离成K+和Cl- | |
| B. | 氧化还原反应的本质是有化合价的升降 | |
| C. | 依据丁达尔效应可将分散系分为溶液、胶体与浊液 | |
| D. | 碱性氧化物均属于金属氧化物 |
1.下列反应的离子方程式正确的是( )
| A. | 大理石和硝酸:CO32-+2H+═H2O+CO2↑ | |
| B. | 铁和稀盐酸:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 稀硫酸和氨水:H++NH3•H2O═NH4++H2O | |
| D. | 碳酸氢钙溶液和盐酸:HCO3-+H+═H2O+CO2↑ |
2.以石墨电极电解200mL CuSO4溶液,电解过程中电子转移物质的量n(e-)与产生气体总体积V(g)(标准状况)的关系如图所示.下列说法中(忽略溶液体积变化)正确的是( )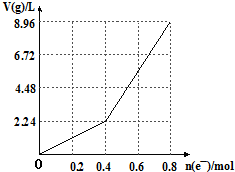

| A. | 电解前CuSO4溶液的物质的量浓度为2mol/L | |
| B. | 电解后所得溶液中c(H+)═2mol/L | |
| C. | 当n(e-)=0.6mol时,V(H2):V(O2)=3:2 | |
| D. | 向电解后的溶液中加入16gCuO,则溶液可恢复为电解前的浓度 |