题目内容
下列化学用语书写正确的是( )
A、氯原子的结构示意图: | ||||||||
B、用电子式表示氯化氢分子的形成过程:H?:
| ||||||||
C、氯化镁的电子式: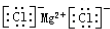 | ||||||||
| D、甲烷的结构式:CH4 |
考点:电子式、化学式或化学符号及名称的综合,原子结构示意图
专题:
分析:A.氯原子的核电荷数=核外电子总数=17,最外层为7个电子;
B.氯化氢为共价化合物,其电子式中不能标出所带电荷;
C.氯化镁为离子化合物,阴阳离子需要标出离子所带电荷,阴离子需要标出最外层电子;
D.用短线代替共用电子对即为甲烷的结构简式,甲烷为正四面体结构.
B.氯化氢为共价化合物,其电子式中不能标出所带电荷;
C.氯化镁为离子化合物,阴阳离子需要标出离子所带电荷,阴离子需要标出最外层电子;
D.用短线代替共用电子对即为甲烷的结构简式,甲烷为正四面体结构.
解答:
解:A.氯原子的核外电子数为17,最外层为7个电子,氯原子正确的原子结构示意图为: ,故A错误;
,故A错误;
B.氯化氢为共价化合物,氯化氢分子中不存在阴阳离子,用氯化氢的形成过程为: ,故B错误;
,故B错误;
C.氯化镁中存在阴阳离子,氯化镁的电子式为: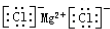 ,故C正确;
,故C正确;
D.CH4为甲烷的分子式,甲烷的结构式为: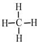 ,故D错误;
,故D错误;
故选C.
 ,故A错误;
,故A错误;B.氯化氢为共价化合物,氯化氢分子中不存在阴阳离子,用氯化氢的形成过程为:
 ,故B错误;
,故B错误;C.氯化镁中存在阴阳离子,氯化镁的电子式为:
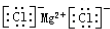 ,故C正确;
,故C正确;D.CH4为甲烷的分子式,甲烷的结构式为:
 ,故D错误;
,故D错误;故选C.
点评:本题考查了原子结构示意图、电子式、结构式等化学用语的表示方法,题目难度中等,注意掌握离子化合物与共价化合物的电子式区别,明确电子式、分子式、结构简式、结构式的区别及正确表示方法.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
0.1mol两种气态烃组成的混合气体完全燃烧,得到0.16mol CO2和3.6g水,下列说法正确的是( )
| A、混合气体中可能有乙烷 |
| B、混合气体一定是甲烷和乙烯 |
| C、混合气体中一定有甲烷 |
| D、混合气体中一定有乙炔 |
白磷和红磷与氧气反应过程与能量的变化关系如图,E表示能量,则下列说法正确的是( )
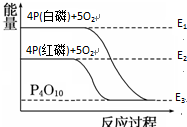

| A、白磷比红磷稳定 |
| B、白磷燃烧是吸热反应 |
| C、红磷转变为白磷是吸热反应 |
| D、红磷燃烧的热化学方程式:4P(s)+5O2(g)=P4O10(s)△H=(E2-E3)kJ/mol |
下列关于乙酸分子的说法不正确的是( )
| A、分子中共含有6个极性共价键 |
| B、分子中不含非极性共价键 |
| C、分子中只含σ键 |
| D、分子中含有1个π键 |
0.75mol RO32-共有30mol电子,则R在周期表中的位置是( )
| A、第2周期 | B、第3周期 |
| C、第ⅣA族 | D、第ⅥA族 |
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、1L 1mol?L-1的NaClO溶液中含ClO-的数目为NA |
| B、78 g 苯含有碳碳双键的数目为3NA |
| C、12.0g熔融的NaHSO4 中含有的阳离子数为0.2NA |
| D、乙烯和乙醇共1 mol,完全燃烧消耗O2的分子数为3NA |
磷酸亚铁锂LiFePO4是一种新型汽车锂离子电池的电极材料,磷酸亚铁锂电池总反应为:FePO4+Li
LiFePO4,下列各种叙述不正确的是( )
| 放电 |
| 充电 |
| A、放电时,Li作负极 |
| B、电解质溶液为非水溶液体系 |
| C、充电时铁元素发生还原反应 |
| D、若用该电池电解饱和食盐水(电解池电极均为惰性电极)当电解池两极共有4480mL气体(标准状况)产生时,该电池消耗锂的质量为1.4 g |