题目内容
元素X的某种原子和元素Y的某种原子质量数相等,两者的质子数之和为34,但前者比后者核内多2个中子,又知元素Y的原子核内质子数和中子数相等,则这两种元素的原子符号分别是 、 .
考点:质子数、中子数、核外电子数及其相互联系
专题:
分析:设X元素原子的质量数为A,质子数为Z(X),中子数为N(X).则Y元素原子的质量数为A,质子数为Z(Y),中子数为N(Y),根据元素X的某种原子和元素Y的某种原子质量数相等,两者的质子数之和为34,但前者比后者核内多2个中子,又知元素Y的原子核内质子数和中子数相等解题.
解答:
解:设X元素原子的质量数为A,质子数为Z(X),中子数为N(X).则Y元素原子的质量数为A,质子数为Z(Y),中子数为N(Y).依题意,有:
Z(X)+Z(Y)=34①
N(X)-N(Y)=2②
Z(Y)=N(Y)③
Z(X)+N(X)=A④
Z(Y)+N(Y)=A⑤
Z将①+②得Z(X)+N(X)=36,代入④中得A=36,由③和⑤求出Z(Y)=N(Y)=18,
所以,Y是氩元素,X是硫元素,即Ar的质子数和质量数分别为18、36,S的质子数和质量数分别为16、36,
故答案为:3616S;3618Ar.
Z(X)+Z(Y)=34①
N(X)-N(Y)=2②
Z(Y)=N(Y)③
Z(X)+N(X)=A④
Z(Y)+N(Y)=A⑤
Z将①+②得Z(X)+N(X)=36,代入④中得A=36,由③和⑤求出Z(Y)=N(Y)=18,
所以,Y是氩元素,X是硫元素,即Ar的质子数和质量数分别为18、36,S的质子数和质量数分别为16、36,
故答案为:3616S;3618Ar.
点评:本题考查原子结构,明确质子数、中子数、核外电子数及其相互联系是解题的关键,题目难度不大.

练习册系列答案
 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目
下列关于元素周期律和元素周期表的说法中正确的是( )
| A、目前发现的所有元素占据了周期表里全部位置,不可能再有新的元素被发现 |
| B、元素的性质随着原子序数的增加而呈周期性变化 |
| C、俄国化学家道尔顿为元素周期表的建立作出了巨大贡献 |
| D、最外层电子数为8的粒子是稀有气体元素的原子 |
一定温度和一定体积的密闭容器中发生如下反应:A2(s)+B2(g)?2AB(g),反应达到平衡状态的标志是( )
| A、V正(B2)═2V逆(AB) |
| B、单位时间内生成2molAB的同时消耗1mol的B2 |
| C、容器内的总压强不随时间而变化 |
| D、气体密度不再随时间变化而变化 |
下列表示对应化学反应的离子方程式正确的是( )
| A、硫酸铝溶液中加入过量氨水 Al3++3OH-=Al(OH)3↓ |
| B、将铁粉加入稀硫酸中:2Fe+6H+=2Fe3++3H2↑ |
| C、NO2与水的反应:3NO2+H2O=2H++2NO3-+NO |
| D、铜片与稀硝酸混合反应:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O |
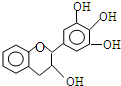 “茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.
“茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中正确的是( )
| A、分子式为C15H12O5 |
| B、遇FeCl3溶液发生显紫色 |
| C、可以和溴水发生反应 |
| D、1molEGC与4molNaOH恰好完全反应 |
 回答下面关于有机实验的问题.
回答下面关于有机实验的问题.