题目内容
17.海洋中有丰富的食品、矿产、能源、药物和水产资源,如图为海水利用的部分过程.下列有关说法不正确的是( )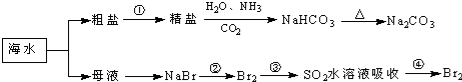
| A. | 工业上通过电解熔融状态MgCl2制取金属镁 | |
| B. | 在第②、④步骤中,溴元素均被氧化 | |
| C. | 用澄清的石灰水可鉴别NaHCO3和Na2CO3 | |
| D. | 制取NaHCO3的反应是利用其溶解度小于NaCl |
分析 A、工业上是电解熔融的氯化镁来制取金属镁;
B、化合价升高的元素在反应中做还原剂被氧化;
C、碳酸钠和碳酸氢钠和氢氧化钙之间均能反应,都会出现白色沉淀;
D、在混合溶液中,溶解度小的物质会先结晶析出.
解答 解:A、工业上是电解熔融的氯化镁来制取金属镁,故A正确;
B、第②步中,溴元素化合价从-1升高到0价,被氧化,第④步中,溴元素化合价从-1升高到0价,被氧化,故B正确;
C、碳酸钠、碳酸氢钠和氢氧化钙之间均能反应,且都会出现白色沉淀,所以用澄清的石灰水不可鉴别NaHCO3和Na2CO3,故C错误;
D、向饱和食盐水中通入氨气以及二氧化碳,溶解度较小的碳酸氢钠会先析出,制取NaHCO3的反应是利用其溶解度小于NaCl,故D正确;
故选C.
点评 本题是一道海水资源的综合利用方面的题目,属于综合知识的考查题,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
7.下列各项叙述中正确的是( )
| A. | 将适量氯化铁饱和溶液滴入沸水中并不断搅拌可制得氢氧化铁胶体 | |
| B. | 若需要使用0.100mol/L的CuSO4溶液480ml,可用12g胆矾及相应容器配制 | |
| C. | 用分液漏斗、烧杯、漏斗架、饱和碳酸钠溶液可除去乙酸乙酯中的乙酸 | |
| D. | 实验室从海带里提取碘的过程是:灼烧、溶解、过滤、萃取 |
8.在密闭容器中充入CO2、CO、H2、C2H6的混合气体m g,若加入足量的Na2O2,充分振荡并不断用电火花引燃至反应完全,测得固体质量增重m g,则相同条件下,CO2与C2H6的体积比为( )
| A. | 4:1 | B. | 2:1 | ||
| C. | 1:1 | D. | 缺少条件,无法计算 |
5.若要在铁片上镀铜,下列叙述中正确的是( )
①将铁片接在电源的正极 ②将铜片接在电源的正极 ③在铁片上发生的反应是Cu2++2e-═Cu ④在铜片上发生的反应是4OH--4e-═2H2O+O2↑ ⑤可用含Fe2+的溶液作电镀液 ⑥可用含Cu2+的溶液作电镀液.
①将铁片接在电源的正极 ②将铜片接在电源的正极 ③在铁片上发生的反应是Cu2++2e-═Cu ④在铜片上发生的反应是4OH--4e-═2H2O+O2↑ ⑤可用含Fe2+的溶液作电镀液 ⑥可用含Cu2+的溶液作电镀液.
| A. | ①③⑥ | B. | ②③⑥ | C. | ①④⑤ | D. | ②③④ |
2.下列关于胶体的叙述正确的是( )
| A. | 将含0.001 mol FeCl3的溶液全部滴到沸水中,可形成0.001 mol Fe(OH)3胶体粒子 | |
| B. | 胶体可以透过半透膜 | |
| C. | 利用丁达尔效应可以区分溶液和胶体 | |
| D. | 直径介于1 nm~100 nm之间的微粒称为胶体 |
6.有关盐类水解的说法不正确的是( )
| A. | 盐类水解是酸碱中和反应的逆反应 | |
| B. | 盐类水解的结果使盐溶液不一定呈中性 | |
| C. | 盐类水解的结果使水的电离程度减小 | |
| D. | 盐类水解的结果使水的电离程度增大 |
8.下表是元素周期表一部分,列出了十个元素在周期表中的位置:
请用化学用语回答下列问题
(1)在③~⑦元素中,原子半径最大的是Ca(填元素符号);
(2)①~⑩中元素最高价氧化物对应的水化物中酸性最强的是HClO4(填物质化学式),呈两性的氢氧化物是Al(OH)3(填物质化学式);
(3)⑦元素的最高价氧化物对应水化物与其氢化物能生成盐M,M中含有的化学键类型有离子键、共价键;
(4)用电子式表示元素③与⑧形成化合物的过程 .
.
(5)写出将⑨元素单质从海水中(离子形式存在)提取所涉及到的三个步骤的离子方程式,第一步:Cl2+2Br-=2Cl-+Br2第二步:Br2+SO2+2H2O=4H++SO42-+2Br-; 第三步Cl2+2Br-=2Cl-+Br2.
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑥ | ⑦ | ||||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(1)在③~⑦元素中,原子半径最大的是Ca(填元素符号);
(2)①~⑩中元素最高价氧化物对应的水化物中酸性最强的是HClO4(填物质化学式),呈两性的氢氧化物是Al(OH)3(填物质化学式);
(3)⑦元素的最高价氧化物对应水化物与其氢化物能生成盐M,M中含有的化学键类型有离子键、共价键;
(4)用电子式表示元素③与⑧形成化合物的过程
 .
.(5)写出将⑨元素单质从海水中(离子形式存在)提取所涉及到的三个步骤的离子方程式,第一步:Cl2+2Br-=2Cl-+Br2第二步:Br2+SO2+2H2O=4H++SO42-+2Br-; 第三步Cl2+2Br-=2Cl-+Br2.