题目内容
4.下列关于电解质溶液中粒子浓度关系的说法不正确的是( )| A. | 0.1 mol/L的NaHCO3溶液中粒子浓度的关系:c(Na+)=c(HCO3-)+c(H2CO3)+2c(CO32-) | |
| B. | 0.2 mol/L的HCl和0.1 mol/L的NH3•H2O等体积混合后溶液中的离子浓度关系: c(Cl-)>c(H+)>c(NH4+)>c(OH-) | |
| C. | pH相同的CH3COONa溶液、Na2CO3溶液、NaOH溶液:c(CH3COONa)>c(Na2CO3)>c(NaOH) | |
| D. | 0.1 mol/L的NaHS溶液中粒子浓度关系:c(S2-)+c(OH-)=(H+)+c(H2S) |
分析 A.碳酸氢钠溶液中存在物料守恒,n(Na)=n(C),钠离子物质的量浓度等于碳元素所有存在形式浓度总和;
B.0.2 mol/L的HCl和0.1 mol/L的NH3•H2O等体积混合得到等浓度的NH4Cl和HCl,分析离子浓度大小比较;
C.CH3COONa溶液、Na2CO3溶液显碱性是盐的水解,NaOH溶液是强碱溶液,PH相同说明氢氧根离子浓度相同,氢氧化钠浓度最小;
D.溶液中电荷守恒和物料守恒计算分析判断.
解答 解:A.0.1 mol/L的NaHCO3溶液中存在物料守恒,粒子浓度的关系:c(Na+)=c(HCO3-)+c(H2CO3)+c(CO32-),故A错误;
B.0.2 mol/L的HCl和0.1 mol/L的NH3•H2O等体积混合得到等浓度的NH4Cl和HCl,溶液中离子浓度大小为c(Cl-)>c(H+)>c(NH4+)>c(OH-),故B正确;
C.CH3COONa溶液、Na2CO3溶液显碱性是盐的水解,NaOH溶液是强碱溶液,PH相同说明氢氧根离子浓度相同,氢氧化钠浓度最小,盐溶液对应酸性越弱水解程度越大,则提供相同氢氧根离子浓度Na2CO3溶液浓度小,则pH相同的CH3COONa溶液、Na2CO3溶液、NaOH溶液:c(CH3COONa)>c(Na2CO3)>c(NaOH),故C正确;
D.0.1 mol/L的NaHS溶液中电荷守恒:2c(S2-)+c(OH-)+c(HS-)=(H+)+c(Na+),溶液中物料守恒为:c(S2-)+c(H2S)+c(HS-)=c(Na+),代入计算得到溶液中粒子浓度关系:c(S2-)+c(OH-)=(H+)+c(H2S),故D正确;
故选A.
点评 本题考查离子浓度大小比较,题目难度中等,本题注意根据反应物的物质的量判断反应物,比较离子浓度大小关系时,常常用到电荷守恒、物料守恒以及质子守恒等方法,做题时注意体会.

| A. | 甲酸 | B. | 乙二酸 | C. | 丙酸 | D. | 丁酸 |
| A. | 含4molSi-O键的二氧化硅晶体中氧原子数为2NA | |
| B. | 标准状况下,含3NA个σ键的甲醛分子所占的体积约为22.4L | |
| C. | 2molNO和1molO2混合,在密闭容器中充分反应,容器内的分子数小于2NA | |
| D. | 1molFe与一定量的硝酸反应,转移的电子数为0.2NA~0.3NA |
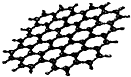 最近,科学家从石墨中分离出来的石墨烯是已知最薄、最坚硬的物质.可以制成纳米材料.其结构如图所示:下列关于石墨烯的说法正确的是( )
最近,科学家从石墨中分离出来的石墨烯是已知最薄、最坚硬的物质.可以制成纳米材料.其结构如图所示:下列关于石墨烯的说法正确的是( )| A. | 属于高分子化合物 | B. | 与金刚石互为同分异构体 | ||
| C. | 性质稳定不能与氧气等物质反应 | D. | 能导电 |

| A. | VB2电极发生的电极反应为:2VB2+11H2O-22e-═V2O5+2B2O3+22H+ | |
| B. | 外电路中电子由c电极流向VB2电极 | |
| C. | 电解过程中,c电极表面先有红色物质析出,后有气泡产生 | |
| D. | 若B装置内的液体体积为100 mL,则CuSO4溶液的物质的量浓度为0.05 mol/L |
| A. | 22.4L | B. | 11.2L | C. | 44.8L | D. | 89.6L |
| A. | 水玻璃可用于生产黏合剂和防火剂 | |
| B. | 误服重金属盐,立即服用牛奶或豆浆可解毒 | |
| C. | 油脂、乙酸乙酯都属于酯类,但不是同系物 | |
| D. | 蔗糖、淀粉、纤维素水解的最终产物都只是葡萄糖 |
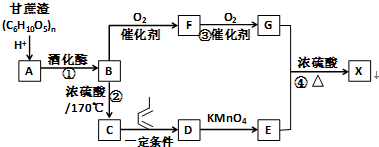
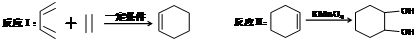
 ,F官能团的名称为醛基,
,F官能团的名称为醛基,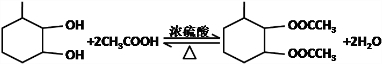 .
. Ⅰ.含六元环Ⅱ.能使溴的四氯化碳溶液褪色
Ⅰ.含六元环Ⅱ.能使溴的四氯化碳溶液褪色 的合成路线为
的合成路线为 .
.