题目内容
能正确表示下列反应的离子方程式是( )
| A、向0.1mol/L的Na2S溶液中加入Agl(s)+S2-?Ag2S(s)+2I- | ||
| B、碳酸钠溶液显碱性的原因:CO32-+2H2O?H2CO3+2OH- | ||
C、一氧化硫通入氯化铁溶液:SO2+Fe3++2H2O═SO
| ||
| D、用醋酸清洗盛放石灰水试剂瓶内壁出现的白色固体:CaCO3+2H+═Ca2++H2O+CO2↑ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.碘化银溶解度大于硫化银;
B.碳酸根离子水解分两步,以第一步为主;
C.电荷不守恒;
D.醋酸为弱电解质,应保留化学式.
B.碳酸根离子水解分两步,以第一步为主;
C.电荷不守恒;
D.醋酸为弱电解质,应保留化学式.
解答:
解:A.向0.1mol/L的Na2S溶液中加入,碘化银溶解度大于硫化银,转化为硫化银沉淀,离子方程式为:Agl(s)+S2-?Ag2S(s)+2I-,故A正确;
B.碳酸钠溶液显碱性的原因,离子方程式:CO32-+H2O?HCO3-+OH-,故B错误;
C.二氧化硫通入氯化铁溶液,离子方程式:SO2+2Fe3++2H2O═SO42-+2Fe2++4H+,故C错误;
D.用醋酸清洗盛放石灰水试剂瓶内壁出现的白色固体,离子方程式:CaCO3+2CH3COOH═Ca2++H2O+CO2↑+2CH3COO-,故D错误;
故选:A.
B.碳酸钠溶液显碱性的原因,离子方程式:CO32-+H2O?HCO3-+OH-,故B错误;
C.二氧化硫通入氯化铁溶液,离子方程式:SO2+2Fe3++2H2O═SO42-+2Fe2++4H+,故C错误;
D.用醋酸清洗盛放石灰水试剂瓶内壁出现的白色固体,离子方程式:CaCO3+2CH3COOH═Ca2++H2O+CO2↑+2CH3COO-,故D错误;
故选:A.
点评:本题考查了离子方程式的书写,题目难度不大,注意沉淀转化的条件是解题的关键.

练习册系列答案
 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案
相关题目
在K37ClO3+6HCl═KCl+3Cl2↑+3H2O反应中( )
| A、氧化产物与还原产物物质的量比是3:1 | ||
B、被氧化的HCl占参加反应HCl总量的
| ||
| C、K37ClO3只有一部分发生还原反应 | ||
| D、反应完成后37Cl存在于KCl |
X、Y、Z、W为四种短周期主族元素,其中X、Z同族,Y、Z同周期,W是短周期主族元素中原子半径最大的,X原子最外层电子数是核外电子层数的3倍,Y的最高正价与最低负价代数和为6.下列说法正确的是( )
| A、Y元素最高价氧化物对应的水化物化学式H2YO4 |
| B、原子半径由大到小的顺序为:Z>Y>W |
| C、W、Z两种元素的气态氢化物中,Z的气态氢化物较稳定 |
| D、X与W形成的两种化合物中,阴、阳离子物质的量之比均为1:2 |
下列装置图及有关说法正确的是( )
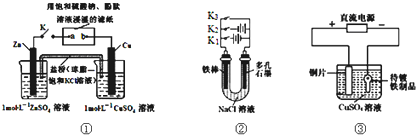

| A、装置①中K键闭合时,片刻后CuSO4溶液中c(Cl-)增大 |
| B、装置①中K键闭合时,片刻后可观察到滤纸a点变红色 |
| C、装置②中铁腐蚀的速度由大到小的顺序是:只闭合K1>只闭合K3>只闭合K2>都断开 |
| D、装置③中当铁制品上析出1.6g铜时,电源负极输出的电子数为0.025NA |
已知某溶液中存在较多的H+、NO3-、SO42-,则该溶液中还可能大量存在的离子组是( )
| A、Na+、Al3+、I- |
| B、NH4+、Cu2+、Cl- |
| C、Mg2+、Cl-、ClO- |
| D、Ba2+、Cl-、Br- |
节能减排,作为我国“十一五”规划中一重要任务,已不仅是政府的一个行动目标,而且还能给企业带来经营上的收入,让城市居民能获得一个较好的生存环境.节能减排更是一个人类解决环境问题的必经之路.下列措施和节能减排无关的是( )
| A、将白炽灯换成节能灯 |
| B、发展利用新能源,如太阳能、氢能、核能等 |
| C、大力植树造林,增加绿色植被 |
| D、少开汽车,采取骑自行车或做公交车 |
用Pt电极电解AgF(aq),电流强度为a A,通电时间为t min,阴极增重m g,阳极上生成标准状况下的纯净气体V L,以q C表示一个电子的电量,Mr示Ag的相对原子质量,则阿伏加德罗常数NA可表示为( )
A、
| ||
B、
| ||
C、
| ||
| D、以上答案都不对 |
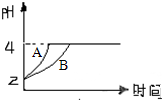 (1)常温下,某纯碱(Na2CO3)溶液中滴入酚酞,溶液呈红色.则该溶液呈
(1)常温下,某纯碱(Na2CO3)溶液中滴入酚酞,溶液呈红色.则该溶液呈