题目内容
【化学一物质结构与性质】金属钛性能优越,被誉为继Fe、Al后应用广泛的“第三金属”.
(1)写出Ti基态原子的电子排布______.
(2)钛能与B、C、N、O等非金属元素形成稳定的化合物.则电负性C______B(选填“>”“<”),第一电离能N>O,原因是______.
(3)月球岩石?玄武岩的主要成分为钛酸亚铁(FeTiO3).FeTiO3与80%的硫酸反应可生成TiOSO4.SO2-4的空间构型为______,其中硫原子采用______杂化,氧原子的价电子排布图为______,任意写出一种SO2-4的等电子体______.
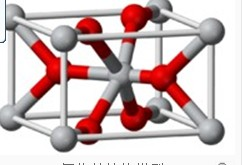
(4)将TiOSO4的稀溶液加热水解后,经进一步反应,可得到钛的某种氧化物.该氧化物的晶胞结构图如图所示.则该氧化物的化学式______(图中钛原子用“O”表示.氧原子用“O”表示)

【答案】分析:(1)根据构造原理写出Ti基态原子的电子排布式;
(2)同一周期元素,元素的电负性随着原子序数的增大而增大,元素的第一电离能随着原子序数的增大而呈增大的趋势,但第IIA族和第VA族元素第一电离能大于其相邻元素,原子的轨道中电子处于半满、全满、全空时比较稳定;
(3)根据价层电子对互斥理论确定其空间构型、杂化方式,氧原子的最外层电子是其价电子,根据其电子排布式写出其价电子排布图,原子个数和价电子数相等的微粒是等电子体;
(4)利用均摊法计算晶胞中含有的各种离子个数,从而确定其化学式.
解答:解:(1)Ti是22号元素,原子核外有22个电子,根据构造原理知Ti基态原子的电子排布式为1s22s22p63s23p63d24s2,故答案为:1s22s22p63s23p63d24s2;
(2)C和B属于同一周期且C的原子序数大于B,所以电负性C>B,N原子中2p轨道处于半充满状态,O原子中2p轨道既不是半充满也不是全空或全满,所以N原子第一电离能比O原子大,故答案为:>;N原子中2p轨道处于半充满比较温度,故第一电离能N>O;
(3)SO42-中价电子数=4+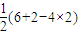 =4,且硫酸根离子中不含孤电子对,所以硫酸根离子呈正四面体构型,采用sp3杂化,氧原子的价电子排布图为
=4,且硫酸根离子中不含孤电子对,所以硫酸根离子呈正四面体构型,采用sp3杂化,氧原子的价电子排布图为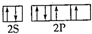 ,SO42-的等电子体有:ClO4- S2O32- PO43-,
,SO42-的等电子体有:ClO4- S2O32- PO43-,
故答案为:正四面体形;sp3;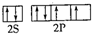 ;ClO4- S2O32- PO43-;
;ClO4- S2O32- PO43-;
(4)Ti原子个数=8× +1=2,O原子个数=2+4×
+1=2,O原子个数=2+4× =4,钛和氧原子个数之比=2:4=1:2,所以其化学式为:TiO2,故答案为:TiO2.
=4,钛和氧原子个数之比=2:4=1:2,所以其化学式为:TiO2,故答案为:TiO2.
点评:本题考查较综合,涉及化学式的确定、电子排布式的书写、电离能、电负性的判断等知识点,电离能、电子排布式的书写、空间构型的判断、杂化方式等知识是考试热点,应重点掌握.
(2)同一周期元素,元素的电负性随着原子序数的增大而增大,元素的第一电离能随着原子序数的增大而呈增大的趋势,但第IIA族和第VA族元素第一电离能大于其相邻元素,原子的轨道中电子处于半满、全满、全空时比较稳定;
(3)根据价层电子对互斥理论确定其空间构型、杂化方式,氧原子的最外层电子是其价电子,根据其电子排布式写出其价电子排布图,原子个数和价电子数相等的微粒是等电子体;
(4)利用均摊法计算晶胞中含有的各种离子个数,从而确定其化学式.
解答:解:(1)Ti是22号元素,原子核外有22个电子,根据构造原理知Ti基态原子的电子排布式为1s22s22p63s23p63d24s2,故答案为:1s22s22p63s23p63d24s2;
(2)C和B属于同一周期且C的原子序数大于B,所以电负性C>B,N原子中2p轨道处于半充满状态,O原子中2p轨道既不是半充满也不是全空或全满,所以N原子第一电离能比O原子大,故答案为:>;N原子中2p轨道处于半充满比较温度,故第一电离能N>O;
(3)SO42-中价电子数=4+
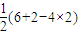 =4,且硫酸根离子中不含孤电子对,所以硫酸根离子呈正四面体构型,采用sp3杂化,氧原子的价电子排布图为
=4,且硫酸根离子中不含孤电子对,所以硫酸根离子呈正四面体构型,采用sp3杂化,氧原子的价电子排布图为 ,SO42-的等电子体有:ClO4- S2O32- PO43-,
,SO42-的等电子体有:ClO4- S2O32- PO43-,故答案为:正四面体形;sp3;
 ;ClO4- S2O32- PO43-;
;ClO4- S2O32- PO43-;(4)Ti原子个数=8×
 +1=2,O原子个数=2+4×
+1=2,O原子个数=2+4× =4,钛和氧原子个数之比=2:4=1:2,所以其化学式为:TiO2,故答案为:TiO2.
=4,钛和氧原子个数之比=2:4=1:2,所以其化学式为:TiO2,故答案为:TiO2.点评:本题考查较综合,涉及化学式的确定、电子排布式的书写、电离能、电负性的判断等知识点,电离能、电子排布式的书写、空间构型的判断、杂化方式等知识是考试热点,应重点掌握.

练习册系列答案
相关题目
(13分)【化学一物质结构与性质】
A、B、M、X、Y、Z是元素周期表中的前 20号元素.且原子序数依次增大。已知它们的部分化台物的性质如下表所示
20号元素.且原子序数依次增大。已知它们的部分化台物的性质如下表所示
| A的最简单氢化物 | B的最简单氢化物 | M的最简单氢化物 | X的氧化物 | Y的最简单氢化物 | Z的最高价氧化物 |
| 含氢量最高的有机物 | 水溶液呈碱性 | 水溶液呈酸性 | 两性氧化物 | 分子呈正四面体构型 | 对应水化物为最强酸 |
(1)写出X原子的电子排布式 。
(2)A、B、M电负性由大到小的排列顺序为 。
(3)Y的最简单氢化物中,Y原子的杂化形式是 。
(4)B的最简单氢化物分子的空间构型是 ,属于 分子(填“极性”或“非极性”)。
(5)比较熔点高低:A最高价氧化物的熔点 Y最高价氧化物的熔点。
(6)判断沸点高低:M氢化物的沸点 Z氢化物的沸点,原因是 。
(13分)【化学一物质结构与性质】
A、B、M、X、Y、Z是元素周期表中的前20号元素.且原子序数依次增大。已知它们的部分化台物的性质如下表所示
|
A的最简单氢化物 |
B的最简单氢化物 |
M的最简单氢化物 |
X的氧化物 |
Y的最简单氢化物 |
Z的最高价氧化物 |
|
含氢量最高的有机物 |
水溶液呈碱性 |
水溶液呈酸性 |
两性氧化物 |
分子呈正四面体构型 |
对应水化物为最强酸 |
回答下列问题
(1)写出X原子的电子排布式 。
(2)A、B、M电负性由大到小的排列顺序为 。
(3)Y的最简单氢化物中,Y原子的杂化形式是 。
(4)B的最简单氢化物分子的空间构型是 ,属于 分子(填“极性”或“非极性”)。
(5)比较熔点高低:A最高价氧化物的熔点 Y最高价氧化物的熔点。
(6)判断沸点高低:M氢化物的沸点 Z氢化物的沸点,原因是 。

 (2013?德州一模)【化学一物质结构与性质】
(2013?德州一模)【化学一物质结构与性质】