题目内容
 图中曲线分别表示相同温度下,压强为P1、P2条件下发生可逆反应:mX(g)+nY(g)?2Z(g)+W(s)的过程.下列说法不正确的是( )
图中曲线分别表示相同温度下,压强为P1、P2条件下发生可逆反应:mX(g)+nY(g)?2Z(g)+W(s)的过程.下列说法不正确的是( )| A、P1>P2 |
| B、m+n=2 |
| C、m+n=3 |
| D、P1、P2下平衡常数相同 |
考点:转化率随温度、压强的变化曲线
专题:化学平衡专题
分析:A.由图示知:增大压强,加快反应速率,但是不会引起化学平衡的移动;
B.根据图象可知:P1、P2压强不同,但化学平衡不移动;
C.总当反应物气体的总体积等于生成物气体的体积,改变压强平衡不移动;
D.化学平衡常数与温度有关,与浓度压强无关.
B.根据图象可知:P1、P2压强不同,但化学平衡不移动;
C.总当反应物气体的总体积等于生成物气体的体积,改变压强平衡不移动;
D.化学平衡常数与温度有关,与浓度压强无关.
解答:
解:A.根据图示可知:增大压强,化学反应速率加快,缩短反应达平衡的时间,所以P1>P2,故A正确;
B.加压,平衡向着气体系数和减小的方向进行,总当反应物气体的总体积等于生成物气体的体积,平衡不移动,该反应图象显示改变压强,平衡不移动,说明反应物气体的总体积等于生成物气体的总体积,即m+n=2,故B正确;
C.该反应图象显示改变压强,平衡不移动,说明反应前后气体总体积不变,即m+n=2,故C错误;
D.该图象表示相同温度下,压强为P1、P2条件下发生可逆反应,因温度未变,所以平衡常数不变,故D正确;
故选C.
B.加压,平衡向着气体系数和减小的方向进行,总当反应物气体的总体积等于生成物气体的体积,平衡不移动,该反应图象显示改变压强,平衡不移动,说明反应物气体的总体积等于生成物气体的总体积,即m+n=2,故B正确;
C.该反应图象显示改变压强,平衡不移动,说明反应前后气体总体积不变,即m+n=2,故C错误;
D.该图象表示相同温度下,压强为P1、P2条件下发生可逆反应,因温度未变,所以平衡常数不变,故D正确;
故选C.
点评:本题考查外界条件对化学平衡移动的影响,题目难度不大,本题注意把握图象的分析,注意从坐标的变化.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目
下列反应不属于置换反应的是( )
| A、CuO+H2=Cu+H2O |
| B、C+2CuO=2Cu+CO2↑ |
| C、Fe2O3+3CO=2Fe+3CO2 |
| D、Fe+CuCl2=Cu+FeCl2 |
下列有关热化学方程式的叙述正确的是( )
| A、已知2H2(g)+O2(g)═2H2O(g);△H=-483.6kJ/mol,则氢气的燃烧热为241.8kJ |
| B、已知C(石墨,s)═C(金刚石,s);△H>0,则金刚石比石墨稳定 |
| C、己知2C(s)+2O2(g)=2CO2(g)△H1;2C(s)+O2(g)=2CO(g)△H2则△H1>△H2 |
| D、含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则表示该反应中和热的热化学方程式为:NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.4kJ/mol |
在一定条件下,在一固定体积的密闭容器中进行下列反应:N2(g)+3H2(g)?2NH3(g),下列能说明反应已达平衡状态标志的是( )
| A、断裂1molN≡N键,同时生成6molN-H键 |
| B、V(H2)=V(NH3)=3:2 |
| C、混合气体的密质不再发生改变 |
| D、容器内混合气体的平均相对分子质量不再发生改变 |
某饱和一元醇和一元醛的混合物共3g,和足量银氨溶液反应后,还原出16.2g银,下列说法正确的是( )
| A、该一元醇也能与银氨溶液反应生成银 |
| B、混合物中一定含有甲醛 |
| C、混合物中醇与醛的物质的量之比为5:3 |
| D、混合物中的一元醛是乙醛 |
下列离子方程式正确的是( )
| A、将氢氧化铁粉末加入氢碘酸中:Fe(OH)3+3H+═Fe3++3H2O |
| B、向次氯酸钙溶液中通入少量二氧化硫:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO |
| C、向碳酸氢钠溶液中滴加过量的氢氧化钡:2HCO3-+Ba2++2OH-═BaCO3↓+H2O+CO32- |
| D、向溴化亚铁溶液中通入少量氯气:2Fe2++Cl2═2Fe3++2Cl- |
设阿伏加德罗常数的值为NA,下列有关说法正确的是( )
| A、0.5mol苯分子中含有C=C双键数为1.5NA |
| B、2.8g乙烯、丙烯和聚乙烯的混合物中所含碳原子数为0.2NA |
| C、标准状况下,2.24L C5H12含有的共用电子对为1.6NA |
| D、1mol甲基(-CH3)所含的电子总数为8NA |
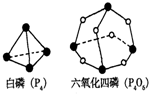 化学反应可视为旧键断裂和新键形成的过程.化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量.已知白磷(P4)和P4O6的分子结构如图所示;现提供以下化学键的键能:P-P 198KJ?mol-1、P-O 360kJ?mol-1、O=O 498kJ?mol-1.则关于1mol P4和3mol O2完全反应(P4+3O2=P4O6)的热效应说法正确的是( )
化学反应可视为旧键断裂和新键形成的过程.化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量.已知白磷(P4)和P4O6的分子结构如图所示;现提供以下化学键的键能:P-P 198KJ?mol-1、P-O 360kJ?mol-1、O=O 498kJ?mol-1.则关于1mol P4和3mol O2完全反应(P4+3O2=P4O6)的热效应说法正确的是( )| A、该反应是吸热反应且吸收热量1638 kJ |
| B、该反应是放热反应且放出热量1638 kJ |
| C、该反应反应物的内能低于产物内能 |
| D、该反应反应物的键能之和高于产物键能之和 |
在相同温度下,有相同体积的甲、乙两容器,甲容器中充入1g N2和1g H2,乙容器中充入2g N2和2g H2.下列叙述中,错误的是( )
| A、化学反应速率:乙>甲 |
| B、平衡后N2的浓度:乙>甲 |
| C、H2的转化率:乙>甲 |
| D、平衡混合气中H2的体积分数:乙>甲 |