题目内容
19.研究证实,CO2也可在酸性水溶液中通过电解生成甲醇,则生成甲醇的反应发生在阴极,该电极反应式是CO2+6H++6e-=CH3OH+H2O..分析 CO2也可在酸性水溶液中通过电解生成甲醇,应为电解池的阴极反应,被还原生成甲醇,据此写出电极反应式.
解答 解:CO2也可在酸性水溶液中通过电解生成甲醇,C元素化合价降低,被还原,应为电解池的阴极反应,电极方程式为CO2+6H++6e-=CH3OH+H2O,
故答案为:阴;CO2+6H++6e-=CH3OH+H2O.
点评 本题考查电化学知识,注意电解池的阴极与阳极上发生的反应的区别.题目难度不大,是基础题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.14C是一种放射性同位素,在一定条件下,14N可转变为14C,下列说法正确的是( )
| A. | 14C和14N互为同位素 | B. | 14N和C60是同素异形体 | ||
| C. | ${\;}_{6}^{14}$C核素中的中子数为8 | D. | 14CO2的摩尔质量为44 |
19. 25℃时,c(CH3COOH)+c(CH3COO-)=0.1mol•L-1的醋酸、醋酸钠混合溶液,c(CH3COOH)、c(CH3COO-)与pH的关系如图所示.下列叙述错误的是( )
25℃时,c(CH3COOH)+c(CH3COO-)=0.1mol•L-1的醋酸、醋酸钠混合溶液,c(CH3COOH)、c(CH3COO-)与pH的关系如图所示.下列叙述错误的是( )
 25℃时,c(CH3COOH)+c(CH3COO-)=0.1mol•L-1的醋酸、醋酸钠混合溶液,c(CH3COOH)、c(CH3COO-)与pH的关系如图所示.下列叙述错误的是( )
25℃时,c(CH3COOH)+c(CH3COO-)=0.1mol•L-1的醋酸、醋酸钠混合溶液,c(CH3COOH)、c(CH3COO-)与pH的关系如图所示.下列叙述错误的是( )| A. | 随pH增大,c(CH3COOH)与c(CH3COO-)的比值减小 | |
| B. | pH=4的溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) | |
| C. | 25℃时,CH3COOH的电离常数K=1×10-2.75 | |
| D. | pH=5的溶液中:c(H+)+c(Na+)+c(CH3COOH)-c(OH-)=0.1 mol•L-1 |
7.某学习小组利用如图装置进行电解氯化铵溶液的实验.其中X为铁,Y为石墨,a为wg质量分数为40%的NH4Cl(滴有酚酞).已知:①氧化性:Cl2>Br2>O2>I2,②NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+3H2O+N2

(l)电解过程中,A 装置中可观察到的现象是X极产生无色气体,Y极产生黄绿色的气体,X极溶液变红.
(2)请选用上述仪器,组装一套检验产生氢气的装置:h→p→q→m→n→j→k→o[按气流方向(用“→”表示),用小写字母表示,装置不重复使用].
(3)某同学认为将E换成装有碱石灰的干燥管也可以达到相同效果,乙同学认为不合理,其理由是碱石灰不能除去混有的氨气,氨气与氧化铜反应产生水蒸气对实验干扰.
(4)设计实验检测阳极产生的气体成分(除水蒸气外).(所选的试剂用字母编号代替)限选试剂:
A、3mol/LNaOH溶液 B、品红 C、酸化的淀粉-KI溶液 D、KBr溶液
(5)电解结束后,加热电解液将NH3完全蒸出,并用水吸收形成200.00mL溶液,取出其中的20.00mL加指示剂后用标准浓度为c mol/L的盐酸溶液滴定,消耗盐酸V mL,则电解制得NH3的产率$\frac{107cV}{80w}$(用化简为整数的含w、c、V的代数式表示).
(6)若实验时反接了正负极,则X极的电极方程式为Fe-2e-=Fe2+.

(l)电解过程中,A 装置中可观察到的现象是X极产生无色气体,Y极产生黄绿色的气体,X极溶液变红.
(2)请选用上述仪器,组装一套检验产生氢气的装置:h→p→q→m→n→j→k→o[按气流方向(用“→”表示),用小写字母表示,装置不重复使用].
(3)某同学认为将E换成装有碱石灰的干燥管也可以达到相同效果,乙同学认为不合理,其理由是碱石灰不能除去混有的氨气,氨气与氧化铜反应产生水蒸气对实验干扰.
(4)设计实验检测阳极产生的气体成分(除水蒸气外).(所选的试剂用字母编号代替)限选试剂:
A、3mol/LNaOH溶液 B、品红 C、酸化的淀粉-KI溶液 D、KBr溶液
| 操作 | 现象和结论 |
| 将混合气体依次通入D(或B),足量的A,然后通入C | D变黄色(或B褪色),则混合气体有氯气;C变蓝,则混合气体含的氧气 |
(6)若实验时反接了正负极,则X极的电极方程式为Fe-2e-=Fe2+.
14.25℃、101kPa下,煤炭、氢气、天然气和甲醇(CH3OH)四种燃料的热值(指一定条件下,单位质量的物质完全燃烧所放出的热量)依次是33kJ•g-1、143kJ•g-1、56kJ•g-1、23kJ•g-1.则下列热化学方程式正确的是( )
| A. | C(s)+$\frac{1}{2}$O2(g)=CO(g)△H=-396 kJ•mol-1 | |
| B. | 2H2(g)+O2(g)=2H2O(l)△H=-286 kJ•mol-1 | |
| C. | CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-896 kJ•mol-1 | |
| D. | CH3OH(l)+O2(g)=CO2(g)+2H2O (l)△H=-736 kJ•mol-1 |
11.根据编号①~⑩代表的元素在周期表中的位置,回答下列问题:
(1)能显+1价,还能显-1价的元素是H(填元素符号);⑦、⑧、⑨三种元素最高价氧化物对应的水化物,碱性由强到弱的顺序排列为NaOH、Mg(OH)2、Al(OH)3(填化学式).
(2)③的单质在空气中充分燃烧的化学方程式是4Li+O2$\frac{\underline{\;\;△\;\;}}{\;}$2Li2O.④与⑥形成的稳定化合物的电子式为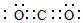 .
.
(3)①、⑤、⑥三种元素形成的一种常见盐的化学式为NH4NO3,其中含有的化学键为离子键和共价键.
(4)高温灼烧由⑦与⑩形成的化合物时,火焰呈黄色.⑧可用于航空航天合金材料的制备,工业上冶炼该单质的化学方程式为MgCl2$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | ② | ||||||
| 2 | ③ | ④ | ⑤ | ⑥ | ||||
| 3 | ⑦ | ⑧ | ⑨ | ⑩ |
(2)③的单质在空气中充分燃烧的化学方程式是4Li+O2$\frac{\underline{\;\;△\;\;}}{\;}$2Li2O.④与⑥形成的稳定化合物的电子式为
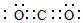 .
.(3)①、⑤、⑥三种元素形成的一种常见盐的化学式为NH4NO3,其中含有的化学键为离子键和共价键.
(4)高温灼烧由⑦与⑩形成的化合物时,火焰呈黄色.⑧可用于航空航天合金材料的制备,工业上冶炼该单质的化学方程式为MgCl2$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑.
8.能正确表示下列反应的离子方程式的是( )
| A. | 将Cl2通入氯化亚铁溶液 Fe2++Cl2═Fe3++2Cl- | |
| B. | 铜与浓硝酸的反应:Cu+4HNO3(浓)═Cu 2++2NO3-+2NO2↑+2H2O | |
| C. | 用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+═Cu2++2Fe2+ | |
| D. | Ca(HCO3)2溶液与过量NaOH溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O |

 .
.