题目内容
16.在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ,下列热化学方程式正确的是( )| A. | CH3OH(l)+O2(g)═CO2(g)+2H2O(l);△H=+725.8kJ/mol | |
| B. | 2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l);△H=-1452kJ/mol | |
| C. | 2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l);△H=-725.8kJ/mol | |
| D. | 2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l);△H=+1452kJ/mol |
分析 1g甲醇燃烧生成CO2和液态水时放热22.68kJ,则1mol甲醇燃烧生成CO2和液态水时放热为22.68kJ×32=725.76kJ,由物质的量与热量成正比可知,2mol甲醇燃烧生成CO2和液态水时放热为1452kJ,结合物质的状态及焓变为负来解答.
解答 解:由信息可知1mol甲醇燃烧生成CO2和液态水时放热为22.68kJ×32=725.76kJ,由物质的量与热量成正比可知,2mol甲醇燃烧生成CO2和液态水时放热为1452kJ,则热化学方程式为CH3OH(l)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(l)△H=-725.8kJ/mol或2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=-1452kJ/mol,
故选B.
点评 本题考查热化学方程式的书写,为高频考点,把握物质的量与热量的关系、焓变的正负为解答的关键,侧重分析与应用能力的考查,注意物质的状态,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.下列说法不正确的是( )
| A. | 硅可用于制造电脑芯片 | B. | 浓H2SO4可用做干燥剂 | ||
| C. | 碳酸氢钠可用于食品的发酵 | D. | 少量金属钠保存在酒精中 |
7.化学与生产、生活、社会密切相关.下列有关说法错误的是( )
| A. | 从海水中可提取镁,电解熔融氯化镁可制得金属镁 | |
| B. | 应用高纯度单质硅制成光导纤维,提高信息传输速度 | |
| C. | 研制高性能的耐磨轮胎,可减少PM2.5等细颗粒物的产生 | |
| D. | 开发二氧化碳制成的全降解塑料,缓解日益严重的“白色污染” |
11.柠檬烯是一种常用香料,其结构简式如图.有关柠檬烯的分析正确的是( )
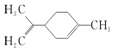

| A. | 它的一氯代物有6种 | |
| B. | 它分子式为:C10H18 | |
| C. | 它的分子中所有的碳原子一定在同一平面上 | |
| D. | 一定条件下,它分别可以发生加成、取代、氧化、加聚等反应 |
8.Q、W、X、Y、Z是原子序数依次增大的短周期元素,X、Y是金属元素,X的焰色反应呈黄色,五种元素核电荷数之和为54,W、Z最外层电子数相同,Z的核电荷数是W的2倍,工业上一般通过电解氧化物的方法获得Y的单质,则下列说法不正确的是( )
| A. | 原子半径:X>Y>Z>Q>W | |
| B. | X、Y和Z三种元素的最高价氧化物的水化物两两间能反应 | |
| C. | 阳离子的氧化性:X>Y | |
| D. | W的最简单氢化物沸点比Z的高 |
5.下列表述中正确的是( )
| A. | 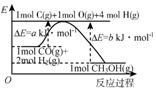 根据图可知合成甲醇的热化学方程式为CO(g)+2H2(g)=CH3OH (g)△H=(b-a)kJ•mol-1 | |
| B. |  图表示2molH2(g)所具有的能量比2mol气态水所具有的能量多483.6kJ | |
| C. | 1molNaOH分别和1molCH3COOH、1molHNO3反应,后者比前者△H小 | |
| D. | 汽油燃烧时将全部的化学能转化为热能 |
6.化学的应用无处不在,下列与化学有关的叙述正确的是( )
| A. | “84消毒液”与含盐酸的沽厕灵混合使用可增强消毒效果 | |
| B. | 《淮南万毕术》所述“白青得铁化为铜”涉及置换反应 | |
| C. | 使用活性炭口罩可减少雾霾对人体的毒害,其原理是活性炭具有杀菌消毒作用 | |
| D. | 用氢氟酸刻蚀玻璃制备工艺品,利用了氢氟酸的氧化性 |
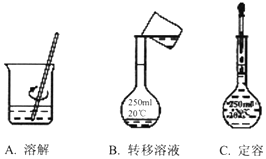 实验室需要配制250mL 1.6mol•L-1的NaOH溶液,请回答下列问题:
实验室需要配制250mL 1.6mol•L-1的NaOH溶液,请回答下列问题: 如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.
如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.