题目内容
20℃时,20mL NaCl饱和溶液质量为24g,将其蒸干后得食盐6.34g,则20℃时,食盐的溶解度为 ,此时食盐饱和溶液的质量分数为 ,物质的量浓度为 .
考点:溶液中溶质的质量分数及相关计算
专题:计算题
分析:计算溶液中水的质量,进而计算100g水能够溶解NaCl质量,即为该温度下NaCl溶解度;溶液质量分数=
×100%;根据n=
计算NaCl的物质的量,再根据c=
计算NaCl溶液物质的量浓度.
| m(溶质) |
| m(溶液) |
| m |
| M |
| n |
| V |
解答:
解:水的质量=24g-6.34g=17.64g,令溶解度为s,则100g:s=17.64g:6.34g,解得s=35.9g;
溶液质量分数w=
×100%=26.4%;
溶液的物质的量浓度c=
=5.42 mol/L,
故答案为:35.9 g;26.4%;5.42mol/L.
溶液质量分数w=
| 6.34g |
| 24g |
溶液的物质的量浓度c=
| ||
| 0.02L |
故答案为:35.9 g;26.4%;5.42mol/L.
点评:本题考查溶液浓度的计算,涉及溶解度、质量分数、物质的量浓度,比较基础,注意对溶解度概念及公式的理解.

练习册系列答案
相关题目
“水过鸭背不留珠”指的是鸭子的羽毛不会被水浸湿,这与鸭子羽毛表面的某种有机物有关,该种有机物可能是( )
| A、油脂 | B、葡萄糖 | C、蔗糖 | D、甘油 |
下列说法或表示方法正确的是( )
| A、日常所用的锌-锰干电池可实现化学能与电能的相互转化 |
| B、由“C(石墨)→C(金刚石)△H=+1.9kJ/mol”可知,金刚石比石墨稳定 |
| C、已知中和热的数值是57.3kJ/mol.若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热量大于57.3kJ |
| D、甲烷和氯水在光照条件下发生取代反应,产物为混合物 |
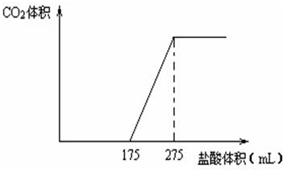 取NaHCO3和Na2O2的固体混合物x g放入一密闭容器中加热至250℃,充分反应后排出所有气体.将反应后的固体分成完全相同的两份,将其中一份投入到足量的BaCl2溶液中,最后可得到3.94g沉淀.另一份溶于适量的水,无气体放出,再向水溶液中缓慢逐滴加入某物质的量浓度的盐酸,产生气体与所加盐酸体积之间的关系如下图所示.试回答下列问题:
取NaHCO3和Na2O2的固体混合物x g放入一密闭容器中加热至250℃,充分反应后排出所有气体.将反应后的固体分成完全相同的两份,将其中一份投入到足量的BaCl2溶液中,最后可得到3.94g沉淀.另一份溶于适量的水,无气体放出,再向水溶液中缓慢逐滴加入某物质的量浓度的盐酸,产生气体与所加盐酸体积之间的关系如下图所示.试回答下列问题: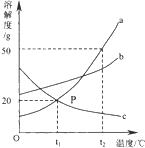 如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答:
如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答: