题目内容
下列各组物质中分子数一定相同的是( )
| A、11.2 L H2和0.5 molCO2 |
| B、18 mL H2O(4℃)和2ⅹ105Pa,27℃32 g O2 |
| C、1 molCO和88 g CO2 |
| D、25℃,22.4 LCl2和含4 mol氧原子的H2SO4 |
考点:物质的量的相关计算
专题:计算题
分析:A.氢气不一定处于标况下,11.2L氢气物质的量不一定是0.5mol;
B.根据m=ρV计算水的质量,根据n=
计算水、氧气的物质的量,若二者物质的量相等,则含有分子数目相等;
C.根据n=
计算二氧化碳的物质的量进行判断;
D.25℃时气体摩尔体积大于22.4L/mol,22.4 LCl2的物质的量小于1mol.
B.根据m=ρV计算水的质量,根据n=
| m |
| M |
C.根据n=
| m |
| M |
D.25℃时气体摩尔体积大于22.4L/mol,22.4 LCl2的物质的量小于1mol.
解答:
解:A.温度、压强影响气体摩尔体积,氢气所处状态的气体摩尔体积不一定是22.4L/mol,11.2L氢气物质的量不一定是0.5mol,与0.5mol二氧化碳含有分子数目不一定相等,故A错误;
B.18 mL H2O的质量为18g,物质的量为1mol,32 g O2的物质的量为1mol,二者含有分子数目相等,故B正确;
C.88g二氧化碳的物质的量为
=2mol,与1molCO含有分子数目不相等,故C错误;
D.含有4mol氧原子的H2SO4的物质的量为1mol,25℃时气体摩尔体积大于22.4L/mol,22.4 LCl2的物质的量小于1mol,二者含有分子数目不相等,故D错误,
故选B.
B.18 mL H2O的质量为18g,物质的量为1mol,32 g O2的物质的量为1mol,二者含有分子数目相等,故B正确;
C.88g二氧化碳的物质的量为
| 88g |
| 44g/mol |
D.含有4mol氧原子的H2SO4的物质的量为1mol,25℃时气体摩尔体积大于22.4L/mol,22.4 LCl2的物质的量小于1mol,二者含有分子数目不相等,故D错误,
故选B.
点评:本题考查物质的量有关计算,注意气体摩尔体积的使用条件与对象,根据PV=nRT理解温度、压强对气体摩尔体积的影响,注意物质的组成、性质以聚集状态等问题.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列关于盐酸与醋酸两种稀溶液的说法正确的是( )
| A、相同浓度的两溶液中c(H+)相同 |
| B、100mL 0.1mol/L的两溶液能中和等物质的量的氢氧化钠 |
| C、相同浓度同体积的两溶液分别与足量的镁反应,生成的气体质量相同 |
| D、两溶液中分别加入少量对应的钠盐固体,c(H+)均明显减小 |
下列离子方程式书写正确的是( )
| A、向碳酸钠溶液中滴加与其溶质的物质的量相等的盐酸:CO32-+2H+═CO2↑+H2O |
| B、用Na2S处理含Hg 2+的废水:Hg2++S2-═HgS↓ |
| C、用Na2CO3溶液处理水垢中的CaSO4:Ca2++CO32-═CaCO3 |
D、邻羟基苯甲酸与足量的NaOH溶液混合: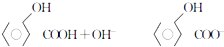 +H2O +H2O |
下列说法①卢瑟福提出的“带核的原子结构模型”认为原子由位于原子中心的原子核和绕核作高速运动的核外电子构成②化学反应中原子之间通过电子转移都达到8电子稳定结构③1123Na的质量数为23,由该原子形成的钠离子的质量数也是23.其中正确的是( )
| A、①②③ | B、①② |
| C、①③ | D、只有① |
下列各项中,含氧原子数不同的是( )
| A、质量比为2:1的SO2和O2 |
| B、9g水和23g乙醇(C2H5OH) |
| C、标准状况下44.8L的一氧化氮和100 ml 5mol/L的硫酸溶液 |
| D、物质的量相同的Na2SO4和FeSO4 |
称取两份铝粉,第一份加入足量的NaOH溶液,第二份加入足量的盐酸溶液,如果要得到相同体积 (同温同压)的氢气,则两份铝粉的质量比是( )
| A、1:1 | B、1:2 |
| C、3:4 | D、2:5 |
石英光导纤维的主要成分是( )
| A、Si |
| B、SiC |
| C、SiO2 |
| D、Na2SiO3 |