题目内容
6.除去下列括号中的杂质(用化学方程式表示)?①MgO(Al2O3)2NaOH+Al2O3=2NaAlO2+H2O
②Na2CO3(NaHCO3)2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
分析 除杂时要除去杂质且不能引进新的杂质,
①MgO和NaOH不反应,Al2O3和NaOH溶液反应生成可溶性的NaAlO2,然后采用过滤方法除去杂质;
②加热条件下Na2CO3不分解,NaHCO3分解生成Na2CO3和CO2、H2O,所以采用加热方法即可除杂.
解答 解:除杂时要除去杂质且不能引进新的杂质,
①MgO和NaOH不反应,Al2O3和NaOH溶液反应生成可溶性的NaAlO2,然后采用过滤方法除去杂质,
反应方程式为2NaOH+Al2O3=2NaAlO2+H2O;
②加热条件下Na2CO3不分解,NaHCO3分解生成Na2CO3和CO2、H2O,所以采用加热方法即可除杂,反应方程式为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,
故答案为:2NaOH+Al2O3=2NaAlO2+H2O; 2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
点评 本题以物质的分离和提纯为载体考查化学方程式的书写,明确物质差异性是解本题关键,注意:除杂时不能引进新的杂质且操作简单,题目难度不大.

练习册系列答案
 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
16.用NA表示阿伏加德罗常数的数值,下列叙述正确的是( )
| A. | 电解精炼铜时,若阳极质量减少32g,则阴极转移的电子的数目为NA(注:粗铜含有Zn、Fe等杂质) | |
| B. | 含0.2mol H2SO4的浓硫酸与足量铜充分反应,生成SO2分子的数目少于0.1NA | |
| C. | 在标况下,22.4L SO3和22.4L C2H4原子个数比为2:3 | |
| D. | 将78g Na2O2与过量CO2反应,CO2转移的电子数为2NA |
14.模拟推理是化学学习中的一种重要方法.下列类推结论中正确的是( )
| 模拟对象 | 类推结论 | |
| A | 2HCl+Mg═MgCl2+H2↑ | H2SO4+2Na═Na2SO4+H2↑ |
| B | Cl2+2Fe2+═2 Fe3++2Cl- | I2+2Fe2+═2Fe3++2I- |
| C | Mg在O2中燃烧生成MgO | Na在O2中燃烧生成Na2O |
| D | Al在NaOH溶液中反应可产生H2 | Mg与NaOH溶液反应也可以产生H2 |
| A. | A | B. | B | C. | C | D. | D |
11.某无色气体,可以使湿润的蓝色石蕊试纸变红,通入澄清石灰水中,石灰水变浑浊,接着又变澄清,将燃着的蜡烛放入盛有该气体的集气瓶中蜡烛熄灭,则该气体( )
| A. | 一定是CO2 | B. | 一定是SO2 | ||
| C. | 可能是CO2或SO2 | D. | 一定是CO2和SO2混合气体 |
18.常温下,下列各组离子在指定环境中能大量共存的是( )
| A. | 在$\frac{c({H}^{+})}{c(O{H}^{-})}$=1013的溶液中:NH4+、Ca2+、Cl-、K+ | |
| B. | Kw/c(OH-)=1.0mol•L-1的溶液中:Mg2+、NO3、NH4+、I- | |
| C. | 中性溶液中:K+、Cl-、Na+、CO32- | |
| D. | 无色溶液中:Fe3+、Cl-、Na+、SCN- |
16.X、Y、Z、W为四种常见的短周期元素.其中Y元素原子核外最外层电子数是其电子层数的3倍,它们在周期表中的相对位置如图所示:
请回答下列问题:
(1)W位于周期表中第三周期,第VIIA族.
(2)X和氢可以构成+1价阳离子,其电子式是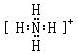 ,Y的气态氢化物的稳定性比Z的气态氢化物的稳定性强(填“强”、或“弱”).
,Y的气态氢化物的稳定性比Z的气态氢化物的稳定性强(填“强”、或“弱”).
(3)工业上将干燥的W单质通入熔融的Z单质中可制得化合物Z2W2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,该反应的化学方程式为2S2Cl2+2H2O═3S↓+SO2↑+4HCl.
(4)①Y和Z可组成一种气态化合物Q,Q能与W的单质在潮湿环境中反应,反应的化学方程式是SO2+Cl2+2H2O=2HCl+H2SO4.
②在一定条件下,化合物Q与Y的单质反应达平衡时有三种气态物质,反应时,每转移4mol电子放热190.0kJ,该反应的热化学方程式是2SO2 (g)+O2(g)?2SO3(g)△H=-190.0 kJ•mol-1.
| X | Y | |
| Z | W |
(1)W位于周期表中第三周期,第VIIA族.
(2)X和氢可以构成+1价阳离子,其电子式是
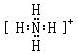 ,Y的气态氢化物的稳定性比Z的气态氢化物的稳定性强(填“强”、或“弱”).
,Y的气态氢化物的稳定性比Z的气态氢化物的稳定性强(填“强”、或“弱”).(3)工业上将干燥的W单质通入熔融的Z单质中可制得化合物Z2W2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,该反应的化学方程式为2S2Cl2+2H2O═3S↓+SO2↑+4HCl.
(4)①Y和Z可组成一种气态化合物Q,Q能与W的单质在潮湿环境中反应,反应的化学方程式是SO2+Cl2+2H2O=2HCl+H2SO4.
②在一定条件下,化合物Q与Y的单质反应达平衡时有三种气态物质,反应时,每转移4mol电子放热190.0kJ,该反应的热化学方程式是2SO2 (g)+O2(g)?2SO3(g)△H=-190.0 kJ•mol-1.
17.下列化合物中同分异构体数目(不考虑立体异构)最少的是( )
| A. | 分子式为C5H12的烃 | B. | 分子式为C4H10O的醇 | ||
| C. | 分子式为C4H8的烯烃 | D. | 分子式为C3H6O2的酯 |
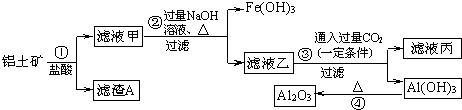
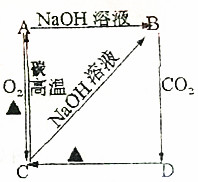 根据如图所示变化关系,请回答下列问题.
根据如图所示变化关系,请回答下列问题.