题目内容
向0.2L某浓度的HNO3溶液中投入2.8g铁粉,结果铁粉全部溶解,同时得到1.12L(标准状况)气体,并测得反应后溶液的pH=1.若反应前后溶液体积变化忽略不计,则下列有关判断中不正确的是( )
| A、反应后的溶液中不存在Fe2+ |
| B、反应后转移的电子数为0.10NA |
| C、1.12L气体全部是NO |
| D、反应后溶液中c(NO3-)=0.85mol?L-1 |
考点:化学方程式的有关计算
专题:计算题
分析:A.测得反应后溶液的pH为l,则硝酸剩余,Fe失去电子变为Fe3+;
B.根据n=
计算Fe的物质的量,结合Fe元素化合价变化计算转移电子;
C.由电子守恒计算N元素在还原产物中的化合价,确定气体为NO或二氧化氮或二者混合物;
D.由题目信息可知,反应后溶液为硝酸铁、硝酸的混合溶液,故溶液中存在3c(Fe3+)+c(H+)=c(NO3-).
B.根据n=
| m |
| M |
C.由电子守恒计算N元素在还原产物中的化合价,确定气体为NO或二氧化氮或二者混合物;
D.由题目信息可知,反应后溶液为硝酸铁、硝酸的混合溶液,故溶液中存在3c(Fe3+)+c(H+)=c(NO3-).
解答:
解:A.测得反应后溶液的pH为l,则硝酸剩余,硝酸可以氧化性Fe2+,故Fe失去电子变为Fe3+,反应后的溶液中不存在Fe2+,故A正确;
B.n(Fe)=
=0.05mol,反应中Fe失去电子变为Fe3+,故转移电子数目=0.05mol×3×NAmol-1=0.15NA,故B错误;
C.n(Fe)=
=0.05mol,n(气体)=
=0.05mol,令N元素在还原产物中化合价为a,则由电子守恒可知,0.05×3=0.05×(5-a),解得a=2,故生成气体为NO,故C正确;
D.反应后溶液为硝酸铁、硝酸的混合溶液,故溶液中有3c(Fe3+)+c(H+)=c(NO3-),根据铁元素守恒由n(Fe)=n(Fe3+)=0.05mol,所以c(Fe3+)=
=0.25mol/L,反应后溶液pH为1,所以c(H+)=0.1mol/L,所以c(NO3-)=0.25mol/L×3+0.1mol/L=0.85mol/L,故D正确;
故选B.
B.n(Fe)=
| 2.8g |
| 56g/mol |
C.n(Fe)=
| 2.8g |
| 56g/mol |
| 1.12L |
| 22.4L/mol |
D.反应后溶液为硝酸铁、硝酸的混合溶液,故溶液中有3c(Fe3+)+c(H+)=c(NO3-),根据铁元素守恒由n(Fe)=n(Fe3+)=0.05mol,所以c(Fe3+)=
| 0.05mol |
| 0.2L |
故选B.
点评:本题考查氧化还原反应的计算,注意利用电子守恒来分析生成的气体,注意D选项中利用电荷守恒解答,题目难度中等.

练习册系列答案
 应用题作业本系列答案
应用题作业本系列答案
相关题目
下列操作完成后,没有沉淀的是( )
| A、向Ca( OH)2与FeCl2混合溶液加足量稀HNO3 |
| B、向Ba( OH)2与KNO3混合溶液加足量稀H2SO4 |
| C、向AgNO3与Na2CO3混合溶液加足量稀HCl |
| D、向BaCl2与Na2CO3混合溶液中加足量AgNO3溶液 |
伞形酮可由雷梭苯乙酮和苹果酸在一定条件下反应值得
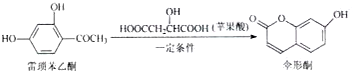
下列有关这三种物质的说法错误的是( )

下列有关这三种物质的说法错误的是( )
| A、雷梭苯乙酮有两种含氧官能团 |
| B、苹果酸和伞形酮分子中均含有1个手性碳原子 |
| C、雷梭苯乙酮和伞形酮都能跟FeCl3溶液发生显色反应 |
| D、1mol伞形酮与足量NaOH溶液反应,最多可消耗2mol NaOH |
下列涉及有机化合物的说法中错误的是( )
| A、乙醇可以转化成乙酸,乙醇和乙酸都能发生取代反应 |
| B、苯和乙烯都能使溴水褪色,其褪色原理是相同的 |
| C、石油裂化的目的主要是为了提高轻质油的产量和质量 |
| D、石油裂解的目的主要是为了获取短链不饱和烯烃 |
将下列物质的水溶液蒸干并灼烧,能得到溶质的是( )
| A、NaHCO3 |
| B、Na2CO3 |
| C、AlCl3 |
| D、NH4HCO3 |
下列分子或离子中,含有孤对电子的是( )
| A、NH4+ |
| B、CH4 |
| C、H2S |
| D、SiH4 |
在A2+3B2=2C的反应中,经过t秒钟后,C的浓度增加了0.6mol/L,在此期间,反应速率V(B=0.45mol/(L?S),则t值为( )
| A、1秒 | B、1.5秒 |
| C、2秒 | D、2.5秒 |
当不慎有大量Cl2扩散到周围空间时,处在该环境中的人可以用浸有一定浓度某种物质的水溶液的毛巾捂住鼻子,以防中毒,该物质最适宜采用的是( )
| A、NaOH |
| B、NaCl |
| C、NaHCO3 |
| D、NH3?H2O |