题目内容
能正确表示下列反应的离子方程式是( )
| A、碳酸氢铵和足量的氢氧化钠溶液反应:NH4++OH-=NH3↑+H2O |
| B、氯化铝溶液中加入过量氨水:Al3++4NH3?H2O=AlO2-+4 NH4++2H2O |
| C、硫代硫酸钠溶液中滴入稀盐酸:S2O32-+2H+=S↓+SO2↑+H2O |
| D、在NaHSO4溶液中滴加Ba(OH)2至中性:H++SO42-+Ba2++OH-=BaSO4↓+H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.漏写碳酸氢根离子与碱的反应;
B.反应生成氢氧化铝和氯化铵;
C.发生氧化还原反应生成S、SO2、H2O;
D.至中性以2:1反应,生成硫酸钡、硫酸钠和水.
B.反应生成氢氧化铝和氯化铵;
C.发生氧化还原反应生成S、SO2、H2O;
D.至中性以2:1反应,生成硫酸钡、硫酸钠和水.
解答:
解:A.碳酸氢铵和足量的氢氧化钠溶液反应的离子反应为HCO3-+NH4++2OH-=NH3.H2O+H2O+CO32-,故A错误;
B.氯化铝溶液中加入过量氨水的离子反应为Al3++3NH3?H2O=Al(OH)3↓+3NH4+,故B错误;
C.硫代硫酸钠溶液中滴入稀盐酸的离子反应为S2O32-+2H+=S↓+SO2↑+H2O,故C正确;
D.在NaHSO4溶液中滴加Ba(OH)2至中性的离子反应为2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,故D错误;
故选C.
B.氯化铝溶液中加入过量氨水的离子反应为Al3++3NH3?H2O=Al(OH)3↓+3NH4+,故B错误;
C.硫代硫酸钠溶液中滴入稀盐酸的离子反应为S2O32-+2H+=S↓+SO2↑+H2O,故C正确;
D.在NaHSO4溶液中滴加Ba(OH)2至中性的离子反应为2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,故D错误;
故选C.
点评:本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重与量有关的离子反应、氧化还原反应的离子反应考查,综合性较强,题目难度不大.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
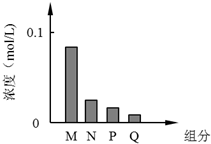 常温下,将10mL 0.2mol/L的一元酸HA与V mL等浓度的NaOH溶液混合.当V=10mL时,所得溶液中部分微粒组成及浓度如图所示.假设溶液体积可以相加,则下列说法正确的是( )
常温下,将10mL 0.2mol/L的一元酸HA与V mL等浓度的NaOH溶液混合.当V=10mL时,所得溶液中部分微粒组成及浓度如图所示.假设溶液体积可以相加,则下列说法正确的是( )| A、图中N表示HA,P表示OH-,Q表示H+ |
| B、若V=10 mL,则pH=7 |
| C、若V<10 mL,则溶液显酸性 |
| D、若V=10 mL,则:c(M)+c(P)=c(Na+) |
下列说法正确的是( )
| A、标准状况下,1mol O2和N2混合气体的体积约为22.4L |
| B、1mol气体的体积约为22.4L |
| C、1mol酒精在标准状况下的体积约为22.4L |
| D、22.4L气体所含分子数一定大于11.2L气体所含的分子数 |
向FeCl3、CuCl2的混合溶液中加入铁粉,充分反应.下列分析合理的是( )
| A、若有固体剩余,则剩余固体一定是Cu |
| B、若有固体剩余,则溶液中一定不含Fe3+和Cu2+ |
| C、若无固体剩余,则溶液中一定有Cu2+和Fe2+ |
| D、若无固体剩余,则溶液中一定有Fe3+ |
高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,是比Cl2、O3、ClO2、KMnO4氧化性更强,无二次污染的绿色水处理剂.工业上是先制得高铁酸钠,然后在低温下,在高铁酸钠溶液中加入KOH至饱和就可析出高铁酸钾(K2FeO4)湿法制备的主要反应方程为:2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O干法制备的主要反应方程为:2FeSO4+4Na2O2=2Na2FeO4+2Na2SO4下列有关说法不正确的是( )
| A、高铁酸钾与水反应时,水发生还原反应 |
| B、湿法中每生成1molNa2FeO4转移3mol电子 |
| C、干法中每生成1molNa2FeO4转移4mol电子 |
| D、K2FeO4处理水时,不仅能消毒杀菌,还能除去H2S、NH3等,并使悬浮杂质沉降 |
用某仪器量一液体体积时,平视时读数为nml,仰视时读数为xml,俯视时读数为yml,若x>n>y,则所用的仪器可能是( )
| A、量筒 | B、酸式滴定管 |
| C、碱式滴定管 | D、容量瓶 |
下列变化属于物理变化的是( )
| A、苏打晶体风化 |
| B、O2在放电条件下变成O3 |
| C、溴水中加入四氯化碳,水层褪色 |
| D、漂白的草帽久置空气中变黄 |